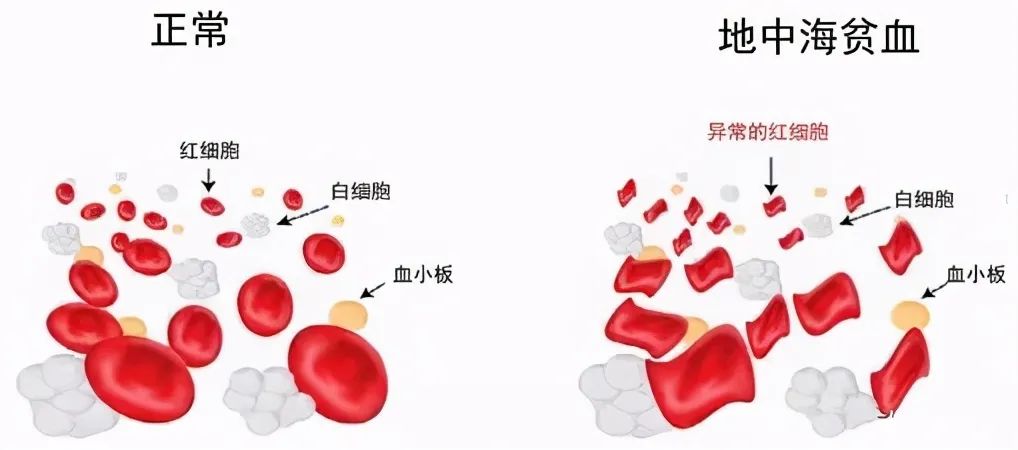
????引子:地中海貧血(β-Thalassemia,地貧)是由于珠蛋白基因突變或者缺失而引起珠蛋白生成障礙,是一種的典型的單基因遺傳病,主要包括α-地貧和β-地貧。地貧基因的攜帶率約占世界人口的1.5%(8000萬~9000萬),每年約誕生68000名患有地貧的兒童,是我國影響最大、發病率最高的遺傳病之一。當前沒有徹底治愈血紅蛋白病的方法,雖然一些病人采用骨髓移植,但其花費巨大,且配型極其困難。
????近年來,基因療法的出現給患者帶來了希望,其最大的優勢在于不需要捐贈,不需要異體移植,而且一次治療可能導致永久性的“治愈”,有望取代目前并不完美的治療方案。?
一、研究目的
????主要目的?
????????評估單劑量靜脈輸注BRL-103(見文末)治療 3-35周歲輸血依賴型β-地中海貧血患者的安全性和有效性。?
????次要目的?
??????? 1.評估外周血白細胞中經基因修飾的目的基因比例。?
??????? 2.評估BRL-103回輸后HbF含量的變化情況。?
?????? 3.評估回輸 BRL-103后對疾病特異性事件和臨床狀態的影響。?
????探索目的?
??????? 1.尋找BRL-103產生療效和預測臨床結果的生物標志物。
????研究疾病:輸血依賴性地中海貧血癥

????倫理:廣西醫科大學第一附屬醫院醫學倫理委員會?
????經費或物資來源:上海邦耀生物科技有限公司?
????研究所處階段:干預性研究?
????實驗設計:單臂
????受試者必須滿足以下所有條件:
??? 1.受試者本人或/且至少需要一位受試者的法定監護人/代理人對本研究和長期隨訪研究已充分了解并自愿簽署書面知情同意書。
??? 2.年齡3-35周歲,性別不限。
??? 3.臨床確診為TDT,基因型主要包括:β0β0,β+β0,βEβ0和β+/β+。TDT定義為地貧患者具有嚴重貧血(Hb持續??? 4.不能接受常規異基因干細胞移植者。
??? 5.成年患者Karnofsky level of performance( KPS)評分≥70分,兒童患者Lansky level of performance(LPS) 評分≥70分。
??? 6.研究者判定受試者身體狀況可以接受自體造血干細胞移植。
??? 7.依從性好,愿意遵守訪視時間安排、試驗計劃、實驗室檢查以及其它試驗步驟。
??? 8.愿意參加長期隨訪研究。
??? 9.育齡受試者研究期間必須采取有效避孕措施。
四、排除標準
????受試者如果滿足下列任何一個條件則不能進入研究:
??? 1.已知對造血干細胞動員劑(plerixafor/G-CSF)、白消安注射液或DMSO過敏者。
??? 2.診斷為復合α地中海貧血。
??? 3.既往接受過基因治療或基因編輯治療。
??? 4.脾切除者。
??? 5.未糾正的出血性疾病。
??? 6.研究者者判定具有臨床意義的細菌、真菌、寄生蟲或病毒感染。
??? 7.存在惡性腫瘤病史或家族史。
??? 8.存在中樞神經系統疾病、心血管系統疾病或精神疾病病史。
??? 9.患有骨髓增生性疾病、內分泌紊亂性疾病或有明顯免疫功能異常者。
??? 10.受試者在篩選前3個月內參加過其他臨床研究并使用藥物者。
??? 11.研究者判定為非脾功能亢進引起的白細胞計數^9/L和/或血小板計數^9/L。
??? 12.國際標準化比值(International normalized ratio,INR)>1.5×正常值上限(Upper limit of normal,ULN)或活化部分凝血活酶時間(Activated Partial Thromboplastin Time,APTT)>1.5×ULN。
??? 13.血清肌酐>1.5×ULN或內生肌酐清除率? 14.谷丙轉氨酶(Alanine aminotransferase,ALT)>3×ULN、谷草轉氨酶(Aspartate aminotransferase,AST)>3×ULN或直接膽紅素> 2×ULN。
??? 15.左心室射血分數(Left Ventricular Ejection FractionL,LVEF)??? 16.乙肝病毒(HBV):HbsAg或HbcAb陽性,核酸檢測陽性者;丙肝病毒(HCV):HCAb陽性,核酸檢測陽性;人類免疫缺陷病毒(Human immunodeficiency virus, HIV)抗體或梅毒螺旋體
(Treponema pallidum, TP)特異性抗體檢查陽性;結核:γ干擾素釋放實驗陽性。
??? 17.受試者存在嚴重的鐵過載,血清鐵蛋白≥5000 ng/ml或者心臟MRI-T2*??? 18.懷孕或哺乳期婦女。
??? 19.研究者認為不適合參加本臨床研究的任何情況。
研究實施時間:2021-11-01至To 2024-11-30?
五、干預措施 :回輸經γ珠蛋白重激活的自體造血干細胞
????
六、研究負責人:賴永榕
??? Email:laiyongrong@hotmail.com

????????博士、教授、博士導師,碩士導師。現任廣西醫科大學一附院大內科副主任、血液科主任、診斷學教研室副主任。擔任中華醫學會血液病學會全國委員、中華醫學會血液病貧血組及造血干細胞移植學組委員、中華醫學會廣西血液病學學會主任委員、《中華血液學雜志》、《?國際輸血及血液學雜志?》、《?臨床血液學雜志》、《內科》、《?廣西醫學》、《廣西醫科大學報》等多家雜志編委。2000年獲得“廣西十百千人才工程”第二層次人選。2011年評為“十一五”廣西醫藥衛生科技工作標兵。2012年被評為全國優秀科技工作者, 2012年全區創先爭優優秀共產黨員稱號,2012年廣西高等學校創先爭優十大先鋒人物稱號,2012年全區衛生系統創先爭優健康衛士稱號。2013年被評為廣西壯族自治區優秀專家。
關于BRL-103
????來自邦耀生物造血干細胞平臺(modiHSC ?)是利用CRISPR相關編輯系統,慢病毒載體等技術對患者的造血干細胞進行基因修飾,修飾后的造血干細胞回輸到患者體內,通過自我更新和分化重建修飾細胞群體,從而達到治療血液系統疾病的目的。
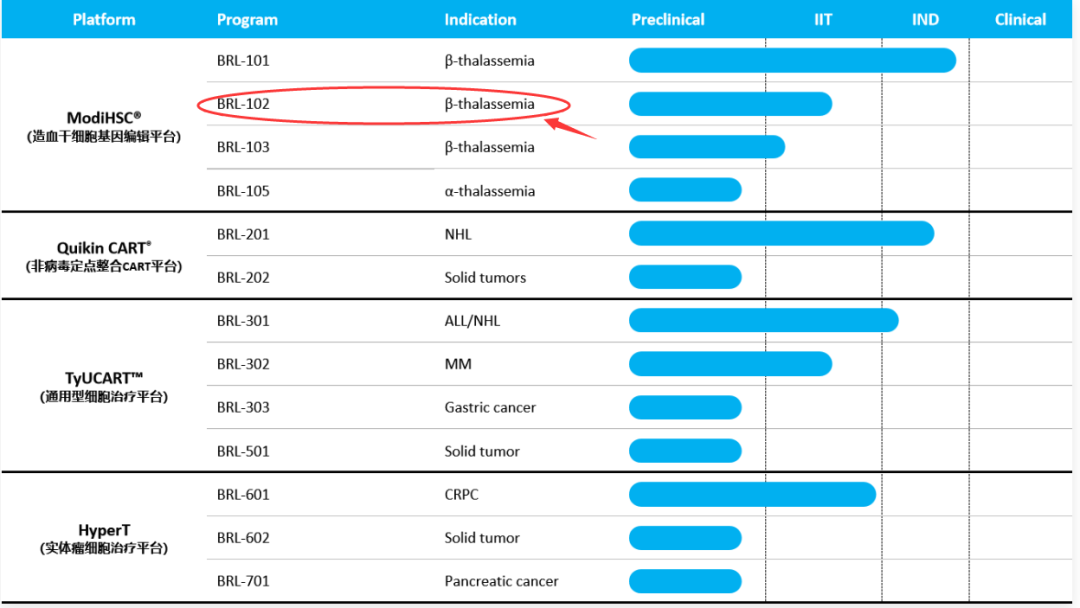
(邦耀生物研發管線-來自公司官網)
編輯:小果果,轉載請注明出處:http://www.448371.com/linchuang/lczm/5926.html
免責聲明:本站所轉載文章來源于其他平臺,主要目的在于分享行業相關知識,傳遞當前最新資訊。圖片、文章版權均屬于原作者所有,如有侵權,請及時告知,我們會在24小時內刪除相關信息。
說明:本站所發布的案例均摘錄于文獻,僅用于科普干細胞與再生醫學相關知識,不作為醫療建議。


 微信掃一掃
微信掃一掃  支付寶掃一掃
支付寶掃一掃