細胞外囊泡(Extracellular Vesicles,EV)是一種由細胞釋放的脂雙層膜包裹的納米囊泡,幾乎所有的細胞都能夠釋放細胞外囊泡。近些年的研究已經證明細胞外囊泡在各種復雜的生理和病理過程中發揮著重要的作用。細胞外囊泡通過攜帶并在細胞間傳遞miRNA參與細胞間信號轉導是其發揮功能的主要策略之一。雖然已有繁多的研究報道細胞外囊泡miRNA在各種生理病理中的功能機制,但是miRNA篩選進入細胞外囊泡的具體機制并不清楚。近日,來自哈佛大學醫學院和加州巴克老化研究所的研究人員通過對細胞駐留和細胞外囊泡富集miRNA的序列分析及具體蛋白和核酸基序的實驗驗證系統性的闡釋了miRNA分選進入細胞外囊泡的具體機制,初步闡釋了細胞外囊泡miRNA的分選系統,相關研究成果以“MicroRNA sequence codes for small extracellular vesicle release and cellular retention”[1]為題于12月22日在Nature在線發表。

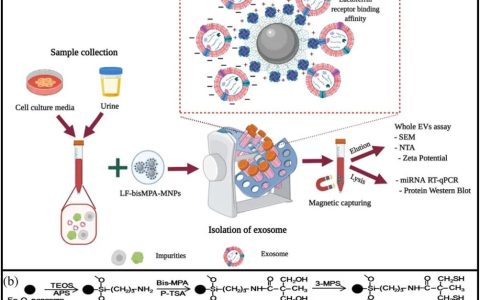
為了研究細胞駐留miRNA和細胞外囊泡富集miRNA的具體特征,研究者們從3T3-L1分化的白色脂肪細胞、棕色脂肪細胞、永生化脂肪細胞以及C2C12(骨骼肌)細胞、SVEC(內皮)細胞和 AML12 細胞(肝細胞)多個小鼠細胞系培養基中通過差速超速離心及超速離心聯合凝膠排阻層析分離純化了細胞外囊泡。并通在經典的驗證實驗證實這些細胞外囊泡直徑分布在50-200 nm,富含經典ALIX、TSG101、CD9 和 CD63標志物,并且相關陰性指標GM130和CANX19呈現陰性。使用基于實時定量PCR (qPCR)的陣列評估分析了分泌的細胞外囊泡及其來源細胞的miRNA組成,結果證實了細胞外囊泡中富集的miRNA和細胞駐留的miRNA種類存在顯著差異(圖 A),并且細胞外囊泡富集的miRNA在不同細胞來源細胞外囊泡中呈現相似趨勢,從而暗示了miRNA進入細胞外囊泡是存在主動分選機制的。

對細胞駐留miRNA和細胞外囊泡富集miRNA的分子種類進行分析發現,有43 個 miRNA 顯著駐留在所有細胞類型的細胞體中,而 13 個 miRNA 在所有細胞類型的細胞外囊泡中都顯著富集。此外,也有許多 miRNA 僅在一種細胞中表現出在細胞或細胞外囊泡中富集,這提示生物體中還存在細胞類型特異性的細胞駐留和細胞外囊泡富集的微調機制。為了闡釋miRNA分選進入細胞外囊泡的具體機制,研究人員對相關miRNA的序列進行了分析并發現了諸多與細胞體駐留和細胞外囊泡富集相關的miRNA基序(圖B)。改變特定miRNA的基序確實可以改變miRNA在細胞或細胞外囊泡中的富集情況(圖C)。利用miRNA進行pull-down,研究者們發現了調控miRNA進入細胞外囊泡的具體分子機器(圖D)。最后,通過實驗,研究者們論證了為miRNA添加特定的基序促進其細胞外囊泡富集并調控受體細胞功能的可行性(圖E)。(此外,該研究還通過詳實的實驗排除了諸如培養基血清、細胞外囊泡分離方法、PCR擴增非均一性原因對該研究結論的潛在干擾。)?
編輯Hzangs按:
大量的研究報道介紹了細胞外囊泡miRNA參與生理病理調控過程,但是由于細胞外囊泡相關miRNA分選機制研究的空白導致細胞外囊泡miRNA功能研究成為了“空中樓閣”。針對細胞外囊泡miRNA是否真的具有廣泛的功能也同樣存在一些質疑聲音。先前已有少量報道介紹特定蛋白可能參與了miRNA進入細胞外囊泡的分選過程,也有零星的文章介紹了個別miRNA進入細胞外囊泡的分選機制[2-6],但是依舊缺少miRNA進入細胞外囊泡機制的系統性闡釋報道。這篇報道通過詳實系統的組學數據以及嚴謹的實驗論證證實了細胞外囊泡miRNA分選系統的存在及工作原理,為深入理解細胞外囊泡miRNA的功能機制提供了可靠的理論依據。
細胞外囊泡作為藥物遞送載體是近兩年產業界開始關注的重要議題之一。由于缺乏對于細胞外囊泡裝載RNA和蛋白機制的理解,工程化細胞外囊泡裝載藥物效率存在嚴重的瓶頸限制,通常只能通過電轉等人為手段實現藥物裝載,如何提高藥物裝載效率是細胞外囊泡作為藥物遞送載體應用于臨床前必須解決的問題。這篇文章所揭示的細胞外囊泡裝載miRNA相關的蛋白機器及核酸基序為優化細胞外囊泡藥物裝載策略和提高細胞外囊泡藥物裝載效率提供了重要的理論支撐和策略選擇。諸如為miRNA或編碼蛋白的mRNA融合特定基序,為蛋白、脂質分子直接共價結合特定基序都是值得嘗試的改善裝載效率的潛在策略。
注:
這篇Nature報道為開源文章,大家可以訪問論文頁面進行閱讀下載:https://www.nature.com/articles/s41586-021-04234-3。
或登錄外泌體之家論壇,在同名貼下載該論文:http://www.exosome.com.cn/forum.php?mod=viewthread&tid=4064&extra=page%3D1。?
參考文獻:
[1] Garcia-MartinR, Wang G, Brandao B B, Zanotto T M, Shah S, Kumar Patel S, Schilling B, Kahn CR. MicroRNA sequence codes for small extracellular vesicle release and cellularretention [J]. Nature, 2021.
[2] Temoche-Diaz M M, Shurtleff M J, Nottingham R M, Yao J,Fadadu R P, Lambowitz A M, Schekman R. Distinct mechanisms of microRNA sortinginto cancer cell-derived extracellular vesicle subtypes [J]. eLife, 2019, 8.
[3] Shurtleff M J, Temoche-Diaz M M, Karfilis K V, Ri S, SchekmanR. Y-box protein 1 is required to sort microRNAs into exosomes in cells and ina cell-free reaction [J]. eLife, 2016, 5.
[4] Cha D J, Franklin J L, Dou Y, Liu Q, Higginbotham J N, DemoryBeckler M, Weaver A M, Vickers K, Prasad N, Levy S, Zhang B, Coffey R J, PattonJ G. KRAS-dependent sorting of miRNA to exosomes [J]. eLife, 2015, 4: e07197.
[5] Villarroya-Beltri C, Gutierrez-Vazquez C, Sanchez-Cabo F,Perez-Hernandez D, Vazquez J, Martin-Cofreces N, Martinez-Herrera D J,Pascual-Montano A, Mittelbrunn M, Sanchez-Madrid F. Sumoylated hnRNPA2B1controls the sorting of miRNAs into exosomes through binding to specific motifs[J]. Nature communications, 2013, 4: 2980.
[6] Statello L, Maugeri M, Garre E, Nawaz M, Wahlgren J,Papadimitriou A, Lundqvist C, Lindfors L, Collen A, Sunnerhagen P, Ragusa M,Purrello M, Di Pietro C, Tigue N, Valadi H. Identification of RNA-bindingproteins in exosomes capable of interacting with different types of RNA:RBP-facilitated transport of RNAs into exosomes [J]. PloS one, 2018, 13(4):e0195969.
編輯:小果果,轉載請注明出處:http://www.448371.com/cells/wmt/7740.html
免責聲明:本站所轉載文章來源于其他平臺,主要目的在于分享行業相關知識,傳遞當前最新資訊。圖片、文章版權均屬于原作者所有,如有侵權,請及時告知,我們會在24小時內刪除相關信息。
說明:本站所發布的案例均摘錄于文獻,僅用于科普干細胞與再生醫學相關知識,不作為醫療建議。


 微信掃一掃
微信掃一掃  支付寶掃一掃
支付寶掃一掃