撰文:南宮明月
來(lái)源:干細(xì)胞者說(shuō)
?
● ? ?● ? ? ●
隨著人類(lèi)的進(jìn)步和發(fā)展,越來(lái)越多前沿科學(xué)研究正在走進(jìn)人們的日常生活,不斷為人們所知、不斷為人們所用。近幾年,一類(lèi)納米尺寸的細(xì)胞囊泡——外泌體(exosome)受到了科學(xué)家們的廣泛關(guān)注。
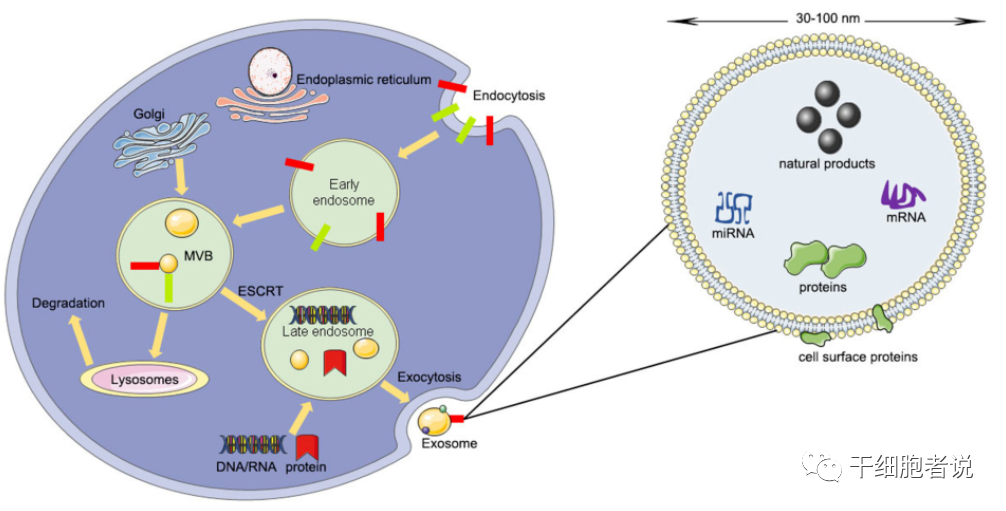
圖 1?外泌體的生物來(lái)源過(guò)程和結(jié)構(gòu)
外泌體,一種直徑約30-150nm的納米級(jí)囊泡,起源于細(xì)胞內(nèi)吞過(guò)程中形成的內(nèi)體,再?gòu)募?xì)胞中釋放到胞外。幾乎所有細(xì)胞都可以分泌外泌體。如果這個(gè)外泌體恰好是干細(xì)胞分泌的,那就叫干細(xì)胞外泌體。如果是腫瘤細(xì)胞分泌的,那就叫腫瘤細(xì)胞外泌體。
?
2013年,外泌體因諾貝爾醫(yī)學(xué)獎(jiǎng)而被眾人知曉,也因此將外泌體研究推向了前所未有的新高潮。外泌體在體液中廣泛存在及易獲得性等特點(diǎn)被譽(yù)為液體活檢”新秀”,成為疾病的精確診斷和治療研究的熱點(diǎn)。
?
–01–
外泌體于1983年首次在體外培養(yǎng)的綿羊紅細(xì)胞上清液中發(fā)現(xiàn)且能被多種細(xì)胞分泌。最初,外泌體被認(rèn)為是細(xì)胞成熟過(guò)程中調(diào)節(jié)膜功能而釋放的多余膜蛋白,是清除細(xì)胞碎片和淘汰細(xì)胞表面分子的細(xì)胞器。直到后來(lái),科學(xué)家們才發(fā)現(xiàn)外泌體在細(xì)胞之間充當(dāng)重要的溝通介質(zhì),進(jìn)而影響細(xì)胞而至組織的生理活動(dòng)。
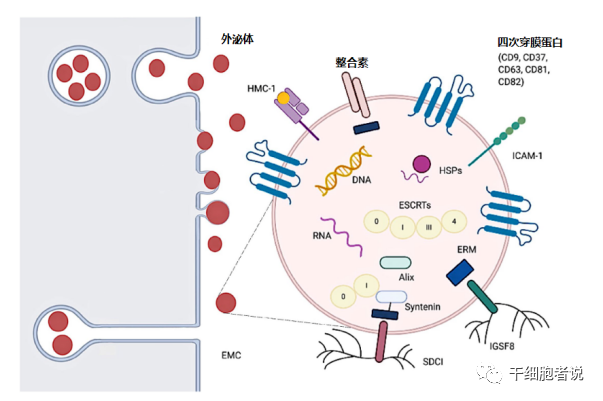
圖 2?外泌體從核內(nèi)體和質(zhì)膜中萌發(fā)
細(xì)胞外囊泡(extracellular vesicles, EVs)?是機(jī)體遠(yuǎn)距離細(xì)胞間交流的一種手段。目前主要被分為3大類(lèi):外泌體、微囊泡和凋亡小體,臨床研究中主要關(guān)注的是外泌體。外泌體就是細(xì)胞外囊泡的一種。自此,外泌體研究成為國(guó)際研究熱點(diǎn),相關(guān)研究駛?cè)肟燔?chē)道。據(jù)統(tǒng)計(jì),Pubmed收錄的外泌體研究相關(guān)文章數(shù)量呈逐年遞增態(tài)勢(shì),一路高歌猛進(jìn),呈現(xiàn)暴風(fēng)增長(zhǎng)。我們帶大家探索一下外泌體目前最火熱的研發(fā)方向。
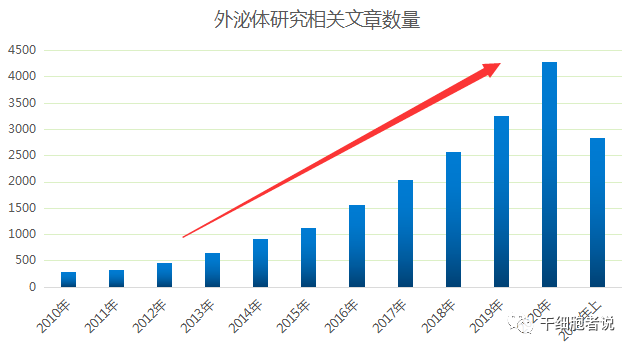
圖3:近十年外泌體研究相關(guān)文章數(shù)量
?
?
–02–
干細(xì)胞外泌體成為研究熱點(diǎn)可能得益于干細(xì)胞研究的蓬勃發(fā)展。間充質(zhì)干細(xì)胞外泌體(MSC-exo)具有免疫調(diào)節(jié)、抗炎和抗纖維化、抑制氧化應(yīng)激、增強(qiáng)血管生成等作用。這主要依賴(lài)于其中的蛋白和核酸組分。例如MSC-exo富含糖酵解相關(guān)酶,可增加ATP的產(chǎn)生,減少組織細(xì)胞死亡,還含有細(xì)胞因子(VEGF、TGF-β1、IL-6、IL-10和HGF等),有利于血管生成和免疫調(diào)節(jié)。
-
2018年5月,F(xiàn)DA批準(zhǔn)了Aegle公司的首個(gè)細(xì)胞外囊泡新藥臨床試驗(yàn)申請(qǐng),以開(kāi)始用于燒傷患者的臨床試驗(yàn)。通過(guò)分離純化MSCs分泌的細(xì)胞外囊泡,用以治療嚴(yán)重的皮膚病,包括燒傷和大皰性表皮松解癥。
-
2019年6月,United Therapeutics宣布其基于外泌體治療支氣管肺發(fā)育不良(BDP)的 I 期試驗(yàn)獲批開(kāi)展。
-
2020年1月,Exopharm宣布了其在人類(lèi)臨床試驗(yàn)中的首次給藥,成為首家測(cè)試外泌體對(duì)傷口愈合能力的公司。Exopharm的Plexaris產(chǎn)品,是無(wú)細(xì)胞的血小板外泌體制劑,在臨床前動(dòng)物研究中,改善了傷口閉合,并減少了疤痕。
干細(xì)胞外泌體可促進(jìn)皮膚創(chuàng)面愈合:促進(jìn)創(chuàng)面局部巨噬細(xì)胞從促炎M1向抑炎M2型轉(zhuǎn)變從而有助于組織修復(fù),抑制肌成纖維細(xì)胞分化和過(guò)度纖維化,從而減少瘢痕形成。間充質(zhì)干細(xì)胞(MSCs)通過(guò)旁分泌效應(yīng),將攜帶細(xì)胞因子和核酸等信號(hào)的外泌體傳遞至鄰近的目標(biāo)細(xì)胞,促進(jìn)損傷部位修復(fù)。
?
?
–03–
所有的細(xì)胞都可以分泌外泌體,機(jī)體的體液內(nèi)和間質(zhì)中均含有大量的外泌體。外泌體被認(rèn)為是疾病診斷的無(wú)創(chuàng)或微創(chuàng)生物標(biāo)志物,具有檢測(cè)包括癌癥在內(nèi)的許多病理狀況的潛力。
?
個(gè)性化和精準(zhǔn)醫(yī)學(xué)的檢測(cè),通常會(huì)使用體液(主要是血液和尿液)的液體活檢正迅速受到關(guān)注,不但方便且對(duì)患者傷害甚微。在液體活檢中主要分析循環(huán)腫瘤細(xì)胞(CTC)、游離DNA(cfDNA)和外泌體。外泌體因穩(wěn)定性高并易于從尿液或血液中收集,是開(kāi)展液體活檢的最佳候選者。
miRNA在機(jī)體內(nèi)起著調(diào)節(jié)作用,故被認(rèn)為有診斷的生物標(biāo)志物的潛力,外泌體miRNA富集的變化可反映生理病理的改變。腫瘤特異性循環(huán)外泌體miRNA已被開(kāi)發(fā)為肺癌的早期診斷生物標(biāo)記。據(jù)報(bào)道,miR-23b-3p,miR-10b-5p和miR-21-5p是非小細(xì)胞肺癌(NSCLC)患者有希望的預(yù)后生物標(biāo)志物。同樣,外泌體也包含來(lái)自宿主細(xì)胞的蛋白質(zhì),因此也具有潛在的生物標(biāo)志物來(lái)源。除了miRNA、蛋白質(zhì)外,來(lái)自癌癥患者的外泌體lncRNA還被定義為新型腫瘤生物標(biāo)記物。
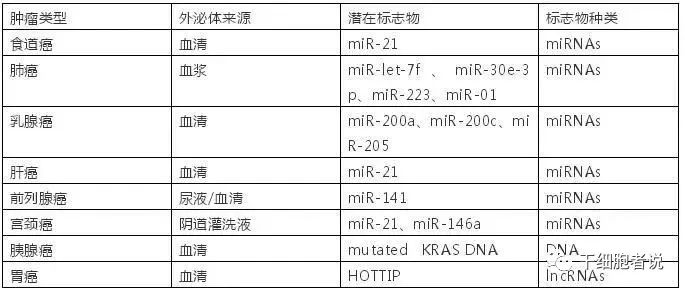
圖4:外泌體內(nèi)容物作為腫瘤的潛在診斷標(biāo)志物
–04–
眼下,外泌體似乎已經(jīng)成為下一個(gè)生物醫(yī)藥的黃金賽道。科學(xué)家們普遍認(rèn)為,外泌體具有其獨(dú)特的生物學(xué)特征,可以作為一種藥物遞送載體。外泌體已經(jīng)成為基因治療的潛在載體,納米尺寸和柔韌性使它們能夠跨越主要的生物屏障,如血腦屏障(BBB)等。與脂質(zhì)體制劑相反,外泌體是天然存在的外分泌型膜囊泡,毒性較低,人體耐受性很好。另外,外泌體的歸巢能力暗示了它們?cè)谒幬镞f送中的潛在效用。例如,源自黑色素瘤的外泌體優(yōu)先進(jìn)入前哨淋巴結(jié),這種歸巢能力可以用作藥物的靶向遞送。
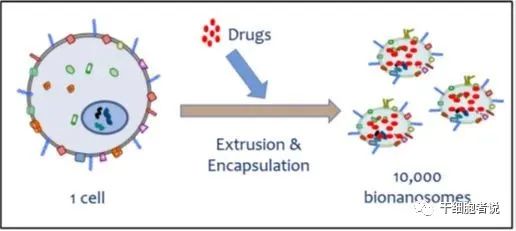
外泌體天然適于運(yùn)輸?shù)鞍踪|(zhì)、mRNA、miRNA、各種非編碼RNA、線粒體DNA以及基因組DNA。利用這一點(diǎn),外泌體可用于遞送siRNA及其他藥物(如親脂性小分子)。比如將抗炎劑姜黃素、抗癌劑阿霉素和紫杉醇等裝載到外泌體中用于相應(yīng)疾病的治療。
基于外泌體的藥物遞送系統(tǒng)在癌癥的治療中具有極大優(yōu)勢(shì),能使得免疫原性和毒性最小化。研究表明,基于外泌體遞送系統(tǒng)的阿霉素的治療功效大大增強(qiáng),并且對(duì)主要器官系統(tǒng)(尤其是心臟)的不良影響明顯減少。
–05–
外泌體具有諸多優(yōu)點(diǎn),在疾病治療中具有難以忽視的價(jià)值。人們對(duì)探索腫瘤中免疫失調(diào)很感興趣,其中包括基于外泌體的腫瘤免疫療法,這有望誕生抗癌疫苗。
腫瘤來(lái)源的外泌體可攜帶抗原,并已被用作針對(duì)腫瘤的免疫反應(yīng)的特異性刺激來(lái)源。B細(xì)胞分泌的外泌體,表達(dá)了MHC-II,從而激活了CD4+T細(xì)胞,而DC細(xì)胞分泌的外泌體表達(dá)了MHC-I,從而激活了CD8+T。這些免疫細(xì)來(lái)源的外泌體可以在臨床前試驗(yàn)和人體試驗(yàn)中展示了可誘導(dǎo)抗腫瘤免疫力,包括結(jié)腸直腸癌、轉(zhuǎn)移性皮膚癌和非小細(xì)胞肺癌等。在I期臨床試驗(yàn)中,用DC外泌體治療晚期非小細(xì)胞肺癌/轉(zhuǎn)移性黑色素瘤患者,顯示出抗腫瘤免疫應(yīng)答和腫瘤消退。在惡性神經(jīng)膠質(zhì)瘤患者中,負(fù)載有腫瘤外泌體的DC細(xì)胞有效地產(chǎn)生了針對(duì)自體腫瘤細(xì)胞的抗腫瘤反應(yīng)。腹水來(lái)源的外泌體與DC細(xì)胞/腫瘤細(xì)胞外泌體一樣有效,可敏化DC細(xì)胞和CTL細(xì)胞,從而在體外殺死自體腫瘤細(xì)胞。結(jié)直腸癌患者的腹水來(lái)源外泌體與GM-CSF聯(lián)合可以有效地誘導(dǎo)晚期結(jié)直腸癌患者有效的CEA特異性抗腫瘤免疫力。
腫瘤來(lái)源的外泌體也表現(xiàn)出強(qiáng)烈的促腫瘤免疫反應(yīng)。腫瘤細(xì)胞外泌體可以抑制T細(xì)胞和NK細(xì)胞活化,且促進(jìn)Treg細(xì)胞功能(如攜帶PD-L1的腫瘤細(xì)胞外泌體可以抑制T細(xì)胞功能促進(jìn)腫瘤生長(zhǎng))。除了Treg細(xì)胞外,腫瘤細(xì)胞外泌體還能抑制DC細(xì)胞活性并促進(jìn)MDSC細(xì)胞的擴(kuò)增。腫瘤細(xì)胞來(lái)源的外泌體也刺激巨噬細(xì)胞向促進(jìn)癌癥的M2期極化。
因此,外泌體在癌癥治療中是一把雙刃劍,同時(shí)發(fā)揮免疫激活和免疫抑制功能。免疫激活作用主要取決于外泌體的抗原呈遞,免疫抑制作用主要取決于其攜帶的配體(如蛋白質(zhì)和miRNA等),可以抑制CTL細(xì)胞的活性或促進(jìn)免疫抑制細(xì)胞增值。唯有知己知彼,方可百戰(zhàn)不殆。
–06–
鑒于外泌體的廣闊應(yīng)用場(chǎng)景,初創(chuàng)企業(yè)如雨后春筍,紛紛涌入這一賽道。部分發(fā)展已然十分成熟的企業(yè),也紛紛立項(xiàng),開(kāi)始積極布局外泌體相關(guān)的業(yè)務(wù)。
如今,眾多企業(yè)正在開(kāi)發(fā)外泌體治療或診斷方法,針對(duì)純天然和工程化的外泌體產(chǎn)品進(jìn)行臨床試驗(yàn)。其中,近1/3的外泌體企業(yè)專(zhuān)注開(kāi)展外泌體診斷相關(guān)業(yè)務(wù);超過(guò)2/3的外泌體企業(yè)專(zhuān)注開(kāi)展外泌體治療相關(guān)的研究。一點(diǎn)也毫不奇怪,許多細(xì)胞企業(yè)也在向外泌體領(lǐng)域拓展。
?
據(jù)動(dòng)脈網(wǎng)不完全統(tǒng)計(jì),通過(guò)梳理全球近50家外泌體企業(yè)的相關(guān)業(yè)務(wù),外泌體相關(guān)企業(yè)主要集中布局在腫瘤(30%)、腦部疾病(16%)、肺部疾病(7%)、皮膚病(5%)、疫苗開(kāi)發(fā)(13%)、醫(yī)美修護(hù)(8%)、肝臟疾病(5%)、腎部疾病(3%)以及基因治療/罕見(jiàn)病(13%)等九個(gè)領(lǐng)域。
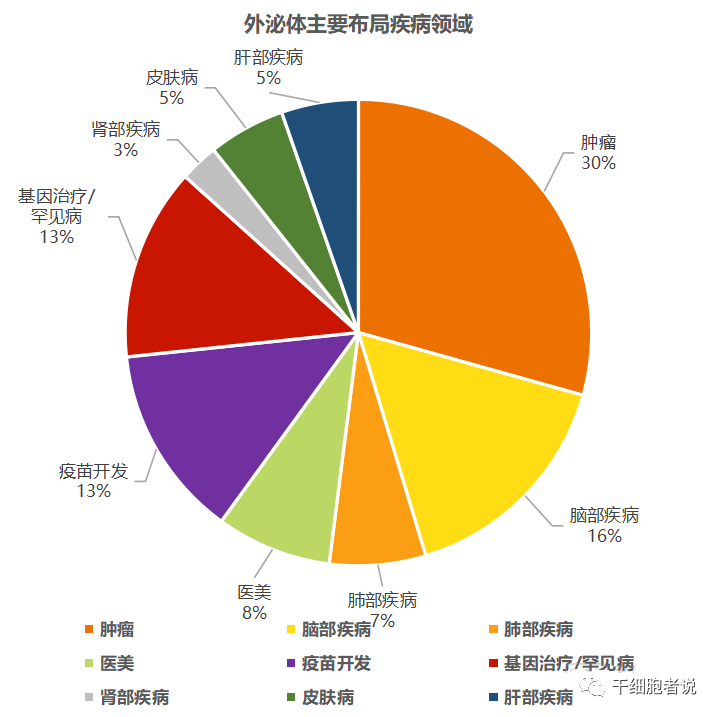
圖6. 外泌體主要布局醫(yī)療領(lǐng)域(數(shù)據(jù)來(lái)自動(dòng)脈網(wǎng))
目前,國(guó)內(nèi)外相關(guān)的研究正如火如荼地進(jìn)行中。外泌體藥物生產(chǎn)工業(yè)化(規(guī)模、純度、成本、一致性和標(biāo)準(zhǔn)化)是目前面臨的重大挑戰(zhàn)。相信未來(lái)幾年,從事外泌體產(chǎn)品開(kāi)發(fā)的項(xiàng)目或企業(yè)將不斷增加,最終外泌體產(chǎn)品將走向商業(yè)化,造福患者。
1. Exosomes: From Garbage Bins to Promising Therapeutic Targets. International journal of molecular sciences,18(3),538.
2. ?Exosomes in cancer development,metastasis,and immunity. Biochimica et biophysica acta. Reviews on cancer,1871(2),455–468.?
3.The potential of exosomes as theragnostics in various clinical situations.Exosomes,467–486.?
4. Review of the Isolation, Characterization, Biological Function, and Multifarious Therapeutic Approaches of Exosomes.Cells,8(4),307.?
5. 吳金恩, & 丁軍濤. (2016). 外泌體生物學(xué)功能及應(yīng)用研究進(jìn)展. 動(dòng)物醫(yī)學(xué)進(jìn)展, 037(012), 90-94.
6. 吳奇, 楊國(guó)棟, 韋夢(mèng)影, 馬雪, & 陳輝. (2016). 外泌體的生物學(xué)功能及其在基因治療中的應(yīng)用. 現(xiàn)代生物醫(yī)學(xué)進(jìn)展(34), 6785-6788.
編輯:小果果,轉(zhuǎn)載請(qǐng)注明出處:http://www.448371.com/cells/wmt/25619.html
免責(zé)聲明:本站所轉(zhuǎn)載文章來(lái)源于其他平臺(tái),主要目的在于分享行業(yè)相關(guān)知識(shí),傳遞當(dāng)前最新資訊。圖片、文章版權(quán)均屬于原作者所有,如有侵權(quán),請(qǐng)及時(shí)告知,我們會(huì)在24小時(shí)內(nèi)刪除相關(guān)信息。
說(shuō)明:本站所發(fā)布的案例均摘錄于文獻(xiàn),僅用于科普干細(xì)胞與再生醫(yī)學(xué)相關(guān)知識(shí),不作為醫(yī)療建議。








 微信掃一掃
微信掃一掃  支付寶掃一掃
支付寶掃一掃