如果有一天,我們身體某一“零件”壞了,而只需要用我們體內(nèi)一個細(xì)胞就可以重新培育出一個新的,那樣的人生會不會很酷炫?
實際上,目前已經(jīng)實現(xiàn)的皮膚移植、器官再造,甚至動物克隆都是人類對于生命可延續(xù)性的探索。而在這之中發(fā)揮著重要作用的正是有“萬能細(xì)胞”之稱的——干細(xì)胞
作為一類具有自我復(fù)制和多向分化潛能的原始細(xì)胞,干細(xì)胞能夠分化成其他細(xì)胞(如肌肉細(xì)胞、神經(jīng)細(xì)胞、脂肪細(xì)胞等),進(jìn)而形成組織、器官乃至完整的個體。因此,醫(yī)學(xué)界稱其為“萬能細(xì)胞”,與干細(xì)胞相關(guān)的醫(yī)學(xué)研究也被稱為“再生醫(yī)學(xué)”。
身懷絕技的干細(xì)胞 你都認(rèn)識嗎?
干細(xì)胞主要存在于胚胎中及成人體內(nèi),根據(jù)其生存階段和分化潛能,分別有不同的分類。如下圖示:
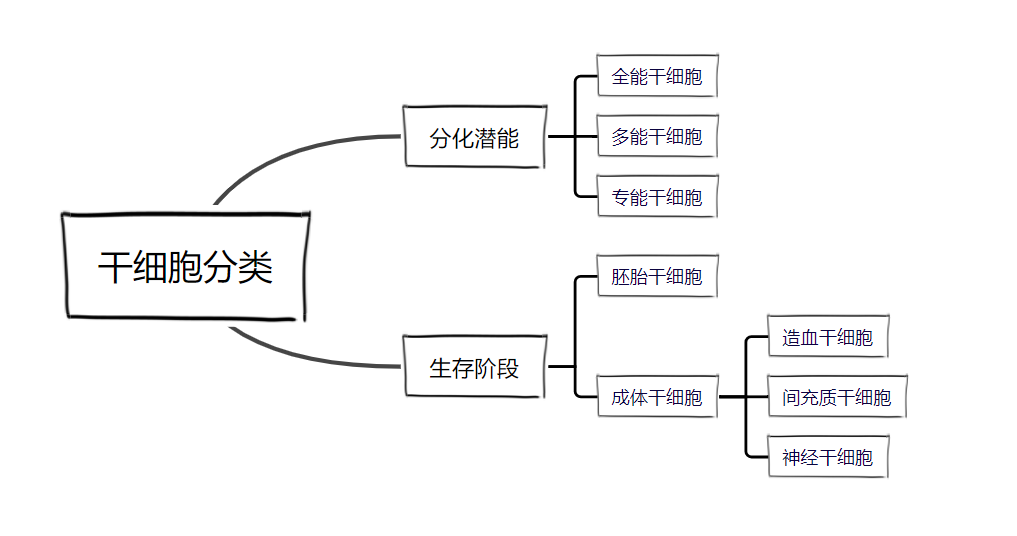
按照生存階段分類,干細(xì)胞分為胚胎干細(xì)胞(Embryonic Stem Cell)和成體干細(xì)胞(Adult Stem Cell)。胚胎干細(xì)胞具有發(fā)育的全能性,能分化出成體動物的所有組織和器官。
而成體干細(xì)胞主要存在于人體的大腦(神經(jīng)干細(xì)胞NeuralStem Cell,NSC)、血液(血液干細(xì)胞Hematopoietic Stem Cell,HSC)、骨髓中(骨髓間充質(zhì)干細(xì)胞Mesen chymal Stem Cell,MSC)以及皮膚中(表皮干細(xì)胞EPidexmisStem Cell)等,用來修復(fù)和維持相應(yīng)部位的組織。
從分化潛能的角度,胚胎干細(xì)胞大多為全能及多能干細(xì)胞,我們熟知的受精卵分裂過程中,到卵裂期32細(xì)胞前的所有細(xì)胞都是全能干細(xì)胞,能夠分化發(fā)育成為各種組織器官的細(xì)胞,最終產(chǎn)生子代個體。
?
而在骨髓中存在的多能造血干細(xì)胞是多能干細(xì)胞的典型例子,它可分化出至少十二種血細(xì)胞,但不能分化出造血系統(tǒng)以外的其它細(xì)胞。
隨著分化的進(jìn)一步加深,干細(xì)胞從全能、多能走向?qū)D埽只瘽撃軇t進(jìn)一步受到限制。
專能細(xì)胞是由多能干細(xì)胞進(jìn)一步分化而成的。它只能向一種類型或密切相關(guān)的兩種類型的APSC多能細(xì)胞分化,比如造血干細(xì)胞可以分化成紅細(xì)胞、白細(xì)胞等各類血細(xì)胞。
將人體細(xì)胞日常運轉(zhuǎn)擬人化的日漫《工作細(xì)胞》中的造血干細(xì)胞
懷里抱著的是剛“出生”不久的紅細(xì)胞,萌萌噠~
隨著干細(xì)胞研究領(lǐng)域向深度和廣度不斷擴展,人們對干細(xì)胞的了解也將更加全面。在醫(yī)學(xué)上針對干細(xì)胞應(yīng)用的探索從未止步,創(chuàng)造了生命科學(xué)的諸多奇跡,比如1996年震驚全球的世界首例克隆羊Dolly,就是從一只母羊的乳腺細(xì)胞中培育而來。
?

右為Dolly本尊,旁邊是她的頭生小羊Bonnie
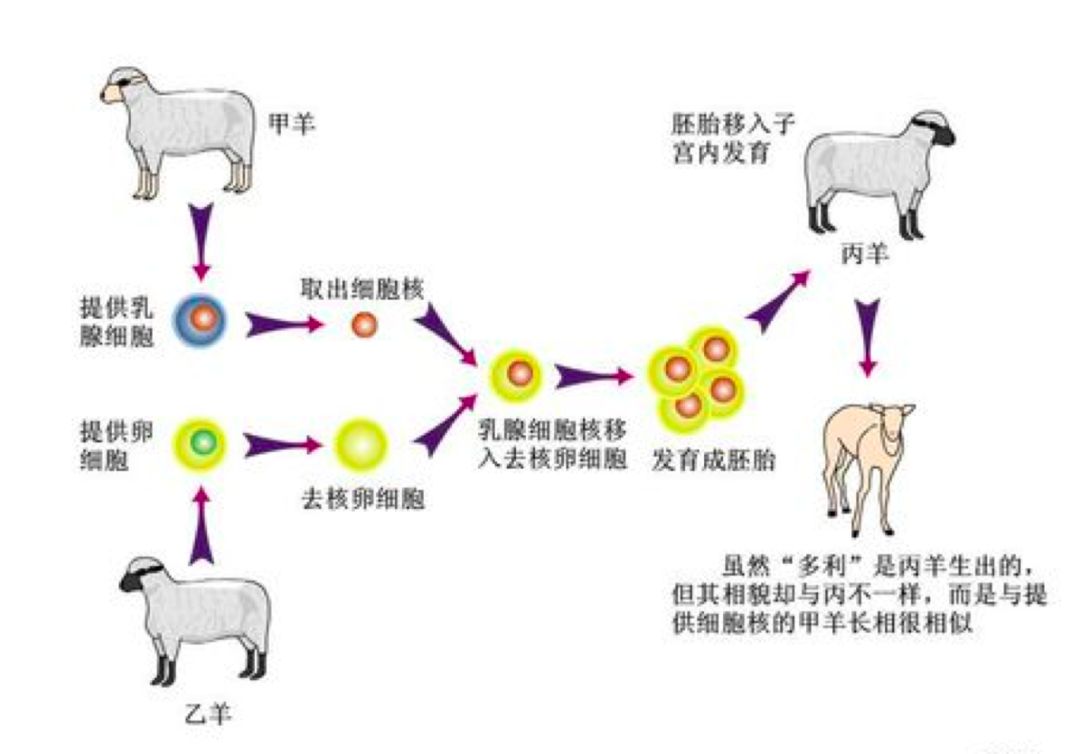
Dolly沒有父親,但有三個母親,一個提供DNA,另一個提供卵子,還有一個負(fù)責(zé)代孕。
干細(xì)胞應(yīng)用 扣響“再生醫(yī)學(xué)”大門!
干細(xì)胞在再生醫(yī)學(xué)領(lǐng)域具有不可估量的醫(yī)學(xué)價值,為許多重大疾病的有效治療提供了新的思路,如果細(xì)胞分化進(jìn)行的順利的話,干細(xì)胞能作為一種細(xì)胞再生資源而存在。目前干細(xì)胞已經(jīng)能夠?qū)崿F(xiàn)部分血液系統(tǒng)疾病和癌癥的治療。
?
擁有超強自愈能力的狼叔
例如,在骨髓移植手術(shù)中,干細(xì)胞被植入骨髓受損的病人體內(nèi),這些未被職能化的細(xì)胞進(jìn)而生成新的骨髓,是自身產(chǎn)生健康的血細(xì)胞。在器官和組織再生方面,若人體皮膚受到創(chuàng)傷,皮膚下的干細(xì)胞能夠用來給燒傷患者進(jìn)行皮膚移植。諾貝爾獎獲得者吉爾伯特認(rèn)為:“用不了50年,人類將能用生物工程的方法培育出人體的所有器官。”?科學(xué)家樂觀地預(yù)料,不久以后,醫(yī)生只要根據(jù)患者自己的需要,用干細(xì)胞,植入預(yù)先由電腦設(shè)計而成的結(jié)構(gòu)支架上,隨著細(xì)胞的分裂和生長,長成的器官或組織就可以植入患者的體內(nèi)。2021年,來自維也納奧地利科學(xué)院的科研團隊,使用人類多能干細(xì)胞成功培養(yǎng)出全球首個體外自組織心臟類器官模型,可自主跳動無需支架支持,且能自我修復(fù)損傷。這項研究發(fā)表在《細(xì)胞》雜志。

2、生物性人造胰腺
東京大學(xué)團隊利用藕狀凝膠開發(fā)人工胰島。東京大學(xué)的竹內(nèi)昌治教授和小澤文智特任研究員等人開發(fā)出了將利用iPS細(xì)胞培養(yǎng)的胰腺細(xì)胞包裹到藕狀凝膠中后進(jìn)行移植的方法。利用該方法將胰腺細(xì)胞移植到糖尿病小鼠體內(nèi)后發(fā)現(xiàn),約半年后血糖值控制到了正常范圍。據(jù)介紹,移植的凝膠可以取出,也不容易發(fā)生免疫排異反應(yīng)。
 將細(xì)胞包裹到藕狀凝膠中的移植片(圖片來源于“客觀日本”網(wǎng)站)
將細(xì)胞包裹到藕狀凝膠中的移植片(圖片來源于“客觀日本”網(wǎng)站)
一項發(fā)表在《Science Translational Medicine》的研究中,研究人員將人類肝細(xì)胞(human hepatocytes)、成纖維細(xì)胞 (fibroblasts) 和內(nèi)皮細(xì)胞索 (endothelial cell cords)以特定的排列模式嵌入到一種能夠被生物降解的水凝膠骨架中。當(dāng)這種人工制造的肝組織被移植到肝臟受損的小鼠腹腔中后,它們能夠生成血管并且與小鼠的循環(huán)系統(tǒng)整合。同時這種人工肝臟組織能夠?qū)π∈蠓置诘拇碳じ闻K再生的信號產(chǎn)生反應(yīng),導(dǎo)致血管生成并且促進(jìn)肝細(xì)胞增殖。
在移植到小鼠體內(nèi)11周后,這些人工肝臟組織不但體積擴展到原來的50倍,并且可以行使正常的肝臟功能。
4、人造腎臟
一項具有突破性進(jìn)展的成果刊登在學(xué)術(shù)期刊《干細(xì)胞報告》上。由曼徹斯特大學(xué)兩位教授領(lǐng)銜的研究團隊先在實驗室培養(yǎng)皿營養(yǎng)液環(huán)境中把人類胚胎干細(xì)胞培養(yǎng)成腎小球,然后將培養(yǎng)出來的腎小球與類似結(jié)締組織的凝膠物混合后注入到實驗小鼠真皮下。
研究人員已經(jīng)能夠?qū)⑷祟惛杉?xì)胞發(fā)展成為“比先前報道的發(fā)現(xiàn)顯著更成熟”的小型腎臟。它具有功能完好的人體血管并能夠過濾宿主血液并產(chǎn)生尿液。

2022年2月8日,國家科技部發(fā)布關(guān)于對國家重點研發(fā)計劃“干細(xì)胞研究與器官修復(fù)”等5個重點專項 2022 年度項目申報指南征求意見的通知。主要任務(wù)圍繞“干細(xì)胞命運調(diào)控及機理”、“干細(xì)胞與器官的發(fā)生與衰老”、“器官的原位再生與機理”、“復(fù)雜器官制造與功能重塑”和“基于干細(xì)胞的疾病模型”等五大方向。涵蓋熱點包括:類器官、器官芯片,外囊泡(外泌體)、干細(xì)胞與器官抗衰老、器官原位再生、干細(xì)胞和生物材料。

從一滴血,到一段血管、一塊軟骨、一片皮膚,再到最終的肝臟、腎臟乃至心臟都是非常復(fù)雜的系統(tǒng),人類的人造器官“夢”依然充滿挑戰(zhàn)。干細(xì)胞技術(shù)的進(jìn)步,人體器官的再生與修復(fù)已不再是科學(xué)幻想。
編輯:小果果,轉(zhuǎn)載請注明出處:http://www.448371.com/cells/gxb/36687.html
免責(zé)聲明:本站所轉(zhuǎn)載文章來源于其他平臺,主要目的在于分享行業(yè)相關(guān)知識,傳遞當(dāng)前最新資訊。圖片、文章版權(quán)均屬于原作者所有,如有侵權(quán),請及時告知,我們會在24小時內(nèi)刪除相關(guān)信息。
說明:本站所發(fā)布的案例均摘錄于文獻(xiàn),僅用于科普干細(xì)胞與再生醫(yī)學(xué)相關(guān)知識,不作為醫(yī)療建議。










 將細(xì)胞包裹到藕狀凝膠中的移植片(圖片來源于“客觀日本”網(wǎng)站)
將細(xì)胞包裹到藕狀凝膠中的移植片(圖片來源于“客觀日本”網(wǎng)站)




 微信掃一掃
微信掃一掃  支付寶掃一掃
支付寶掃一掃 





