生物制藥行業始于19世紀末,至今巴經歷了四次浪潮,逐漸發展出以靶點為核心的研發道路。伴隨著全球藥企、研發機構、高校對于生物醫藥領域不停歇的探索,近些茸創新藥取得了許多重暗成果:首個完整無間隱的人類基因組序列測序的成功、CAR-T細胞療法上市、人工智能輔助藥物設計技術的應用、CRISPR/Cas9技術的使用等。不斷涌現的新興技術與靶點為全球創新藥的發展注入新的活力,也意味著人類對于生物醫藥領域版固的持續拓展。
在全球創新藥蓬勃發展的大環境下,中國藥企也正在探索屬于自己的創新藥研發道路。過去20年,申國醫藥市場憑借醫改推迪和醫保擴窯,從只占全球市場的2%一躍成為僅次于美國的全球第二大醫藥市場。從市場銷售規模看,創新藥僅占申國醫院藥物銷售市場的25%。但隨著仿制藥一致性評價、帶量采購等政策的開展,仿制藥的發展空間越來越窄,發展創新藥成為申國藥企的重點。
然而,創新藥的研發需要極高的研發能力以及巨額的供應資金,創新藥的商業化亦需要草富的專業知識以及強大的營銷能力。長久以來,申國創新藥既不具備有利的外部環境的支持,也不具有自我向上突破的實力與動力,行業發展曼限。自2016年《藥品注冊管理辦法》修訂后,申國創新藥正式進入發展“快車道”。國家政府對于創新藥的重視、資本對于創新藥企業的關注推動申圄創新藥的發展:申國創新藥項目井噴式增妖、創新藥研發政策不斷規范、創新藥市場日益擴大以及申國創新藥企業在各個上市板塊涌現。2020茸的新冠疫情爆發后,國產新冠疫苗的快速上市,無疑是申國創新藥企業交上的一份令人滿意的答卷,申國創新藥已經起航。
近十年,為改變我國醫藥行業長久落后的現狀,一系列政策不斷出臺,中國醫藥行業可謂發生了巨變,同時資本和人才也提供了巨大助力。由此,中國創新藥行業發展環境迎來重大利好,行業發展處處煥發勃勃生機。
受制于時代發展水平的限制,過去我國對藥物研發創新能力沒有給予足夠重視,醫藥相關政策也沒有充分表現出鼓勵創新的導向,仿制藥往往是企業的第一選擇。近些年政府發布了一系列對創新藥利好的政策,以推動創新藥企的發展。從臨床、申報上市到落地使用的全流程,多種政策共同發力為中國創新藥的快速發展營造出良好環境,為創新藥發展奠定了基石。
醫藥行業的快速發展使得越來越多的資本關注到醫藥市場,一級市場表現活躍。二級市場也突破性地對上市規則進行改革,降低了對醫藥行業的上市要求,進一步推動了創新藥行業欣欣向榮的局面。更多資本的流入為我國創新藥的啟動提供了充足的動力。
創新人才是創新藥研發的內在核心,人才引進政策的推出為創新藥發展做好了充分鋪墊。近年來生物醫藥園區為引入優質人才,制定了優厚的人才引進政策,吸引一批又一批優質醫藥人才回國進行創業,為中國創新藥行業注入新鮮血液。

近年來,政府頒布和改革了多項政策以支持創新藥的快速發展,其中包括特殊審批管理條例、先行區政策及醫保政策。
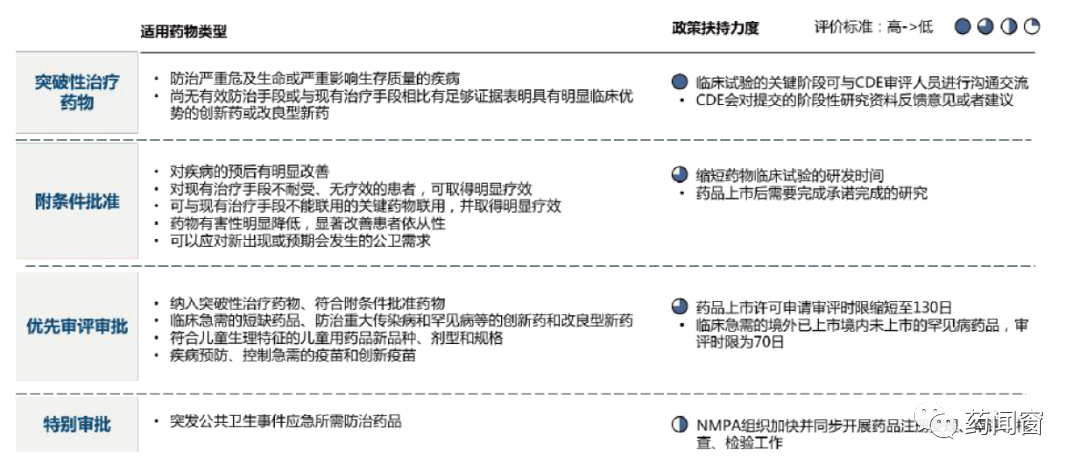
以鼓勵藥品創新,提升藥品質量為導向,國家陸續出臺了一系列針對新藥注冊的特殊審批管理規定,在加快新藥注冊步伐上取得了良好效果。2020年新修訂的《藥品注冊管理辦法》頒布,明確建立藥品加快上市注冊制度,支持以臨床價值為導向的藥物創新。《藥品注冊管理辦法》設立了突破性治療藥物、附條件批準、優先審評審批、特別審批四個加快通道,并明確了每個通道的納入范圍、程序、支持政策等要求(如圖1)。
圖1 ?新藥上市加速審評方式

建設先行區是我國對加速創新藥行業發展的另一大政策創新模式,其能夠通過臨床使用國外已上市、國內未上市的藥物,產生真實世界數據,達到加速藥物上市的目的。2013年2月,海南博鰲國際醫療旅游先行區成立,允許臨床急需的藥品藥械在指定醫療機構先行先試。
2015年大灣區概念提出,2019年2月大灣區發展規劃綱要發布。海南博鰲樂城和大灣區的建立成功打造了與全球醫療資源高度協同接軌的特區。
截至目前,博鰲樂城和大灣區的先行政策已經助力多款藥物臨床使用及上市。2020年3月,我國首個使用境內真實世界數據的醫療器械產品艾爾建“青光眼引流管”獲批上市,其在注冊中使用了在海南博鰲樂城先行區收集的臨床真實世界證據進行人種差異評價。2021年1月,強生全視Catalys飛秒激光眼科治療系統基于博鰲樂城真實世界數據獲批上市,成為繼青光眼引流管之后第二例使用臨床真實世界證據輔助臨床評價獲批的創新型醫療器械產品。
2021年3月,Blueprint ?Medicines普拉替尼膠囊成為首個真實世界數據輔助臨床評價獲批上市的藥品。2021年4月,基于大灣區“港澳藥械通”政策的落地實施,首個藥品強生的“抗D免疫球蛋白注射液”和首個醫療器械“磁力可控延長鐵棒”開始在深圳臨床使用,這是第一款與香港特別行政區同步的新藥。同月歐康維視OT-401的新藥上市申請正式獲NMPA受理,是首個完全基于先行區真實世界數據(博鰲樂城)申報的新藥。
先行區能夠助力多款藥物臨床使用及上市的原因在于先行區具有許多獨特的福利政策。
以博鰲樂城為例,一是特許藥械貿易自由便利,允許使用國際前沿、未在國內上市過的新藥品、新器械。同時對于國外已上市國內未上市的臨床急需特許藥械,審批時間縮短至3個工作日。
二是開放真實數據應用研究,設立真實世界數據研究中,向國外已上市國內未上市的臨床急需進口藥械產品,在真實臨床環境下使用產生數據,并支持藥物在中國的獲批上市。
三是將醫療和藥品二合一監管,博鰲樂城創立了國內第一家由衛生部門和藥監部門共同設立的醫療藥品監管機構,使政府履行職能更加順暢,實現業務協同、信息互通,資源共享,避免多頭監管,形成監管合力,提高監管效率。從研發、臨床試驗、審批、上市使用等多個環節都為新藥提供了極大的政策紅利。

除藥品審批和先行區政策之外,國家對原有的醫保政策也作出了大刀闊斧的改革,以適應和推動創新藥的發展。
首先是對醫保目錄的調整時間進行了改革。以往醫保目錄調整時間間隔較長,不利于新藥進入。國家醫保局近年來逐漸建立起醫保目錄動態調整機制,原則上每年對醫保目錄調整一次。
其次是對醫保目錄的藥品準入路徑也進行了調整。伴隨著國家談判的發展進程,從2017年開始,談判準入逐漸成為目錄調整的重要方式。2019年醫保目錄調整方案明確規定我國醫療保障目錄藥品調整的準入路徑分為常規準入和談判準入兩種。在滿足有效性、安全性等前提下,價格(費用)與藥品目錄內現有品種相當或較低的,通過常規方式納入目錄;價格較高或對醫保基金影響較大的專利獨家藥品應當通過談判方式準入。近些年,談判準入逐漸成為藥品調入的主流。根據醫藥魔方
數據統計,2017年,國家醫保目錄通過常規準入的方式調入的藥品數量還有339種,到2021年國家醫保目錄通過常規準入的方式調入的藥品數量已經下降為7種,而通過談判準入的方式調入的藥品數量從2017年的44種上升為2021年的67種。隨著醫保制度的改革,創新藥逐漸成為醫保談判的主流。

根據醫藥魔方數據庫統計已披露的投融資數據,2013年至2021年中國創新藥領域在投資案例數量有了突破性的增長,在投資金額上也呈現出逐年上升的趨勢。與2013年相比,2021年融資案例數增長超13倍,融資總金額超17倍(如圖2)。
圖2 ?2013-2021年中國創新藥企業投融資情況
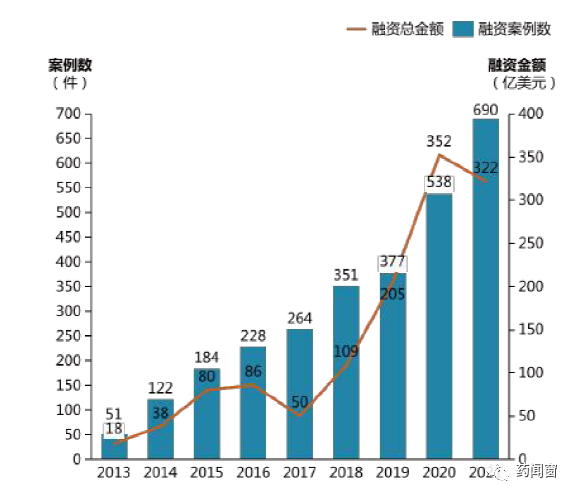

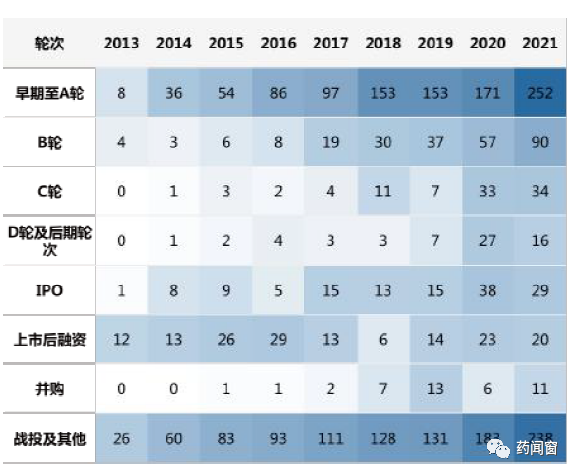
除了融資金額和融資數量的增長,一級市場的融資輪次也愈發早期。早期至A輪階段的融資案例數由2013年的8件突破增長到2021年的252件,B輪融資也快速增長。資本對于創新藥企業更加關注早期(如圖3)。
圖3 ?中國創新藥企業融資熱力圖

除一級市場表現活躍外,二級市場在交易所上市規則的改革與創新下也被大大激發活力,推動了醫藥企業的發展。
2018年4月30日,香港交易所新制訂的《上市規則》生效,新規則規定接受同股不同權企業上市以及允許尚未盈利或者沒有收入的生物科技公司赴港上市。港交所上市制度的改革給諸多擬上市企業提供了赴港上市的機會和可能。
2019年6月13日,上海證券交易所科創板正式開板,允許未盈利企業上市,其上市標準靈活,醫藥企業表現佳,產業鏈表現出細分子行業相對更豐富的特征。港股主板的改革和上交所科創板的創立,為生物醫藥公司的上市提供了有利支持,近些年涌現出一批在港股與科創板上市的創新藥企業。據統計,2018-2021年共有75家企業通過港股及科創板上市,融資總金額達到257.5億美元。

創新藥的研發需要資本的支持,也離不開具有研發能力的人才。創新人才是新藥研發的驅動力。隨著國家逐漸重視生物醫藥產業的發展,各地的生物醫藥產業園區、工業園區紛紛推出了生物醫藥行業人才的引進優惠政策,吸引人才,提供創業支持。
對于生物醫藥行業的高級人才,通常給予購房補貼、各種評審綠色通道、落戶優惠、子女入學、社保醫保優惠等政策吸引其入住園區。對于應屆畢業生,在招聘、實習、落戶等方面給予便利,設立生活補貼,吸引其加入園區企業。而在創業支持方面,園區通常會提供以下支持途徑:一是設立相應計劃,對于不同階段項目的新藥研發與轉化提供資金支持;二是對認定的高新生物醫藥
企業提供生產、研發用地的建設支持等,幫助初創企業更好地建設公司;三是為初創企業提供投融資幫助,對于投資機構設立獎勵等方式,吸引投資機構投資園區內部。
以蘇州工業園區舉例,出臺了《關于加快集聚生物醫藥產業人才的若干措施》共15條全方面的措施。其中例如,措施規定對于生物醫藥人才開通綠色通道,優先享受園區人才優購房、人才優租房和虛擬優租房政策;支持生物醫藥重點企業引進碩士、博士應屆畢業生人才,給予碩士每年3萬元、博士每年4萬元,累計不超過3年的人才補貼;對于入選科技領軍人才創新創業工程的生物醫藥人才提供創新創業資助,最高補貼資助可達5000萬元且頂尖人才補貼金額上不封頂。

受益于政策、資本、人才等多因素共振,中國創新藥企業蓬勃發展,在市場和研發端都有較好表現。在市場端,上市創新藥數量明顯增長,其中國產創新藥數量大副曾多,且在藥品銷售中,隨著上市創新藥數量的增多,中國醫藥市場創新藥銷售占比不斷提高,同時國產創新藥也逐漸進入市場,份額逐年增長。在研發端,中國創新藥企業創新能力顯著增強,近五年來不僅在創新IND和NDA數量上升,同時FIC能力也有了快速發展,并且中國創新藥企業研發能力也逐步被國外企業認可,License out項目逐年增長,還出現了大金額交易事件。
編輯:小果果,轉載請注明出處:http://www.448371.com/zixun/hydt/34688.html
免責聲明:本站所轉載文章來源于其他平臺,主要目的在于分享行業相關知識,傳遞當前最新資訊。圖片、文章版權均屬于原作者所有,如有侵權,請及時告知,我們會在24小時內刪除相關信息。
說明:本站所發布的案例均摘錄于文獻,僅用于科普干細胞與再生醫學相關知識,不作為醫療建議。


 微信掃一掃
微信掃一掃  支付寶掃一掃
支付寶掃一掃