今日,石藥集團宣布,經中華人民共和國國家衛生健康委員會提出建議,國家藥品監督管理局組織論證同意,其自主研發的新型冠狀病毒mRNA疫苗SYS6006在中國納入緊急使用,用于預防新型冠狀病毒(SARS-CoV-2)感染引起的疾病(COVID-19)。這是國內首個獲批使用的新冠mRNA疫苗。
?

SYS6006作為國產mRNA新冠疫苗,涵蓋了Omicron BA.5突變株核心突變位點,于2022年4月獲得國家藥監局的應急批準進行臨床試驗,目前已在國內完成I、II期和序貫加強免疫臨床研究,超5500人研究結果已經證明了其安全性、免疫原性和保護效力。
從作用效果而言,加強接種1劑SYS6006后,14天的針對Omicron BA.5中和抗體的幾何平均滴度(GMT)為236,是加強接種前的83倍。在滅活疫苗2劑或3劑基礎上接種1劑SYS6006的序貫加強免疫,SYS6006顯示出對Omicron BA.5、BF.7、BQ.1.1、XBB.1.5、CH.1.1毒株有很好的交叉中和作用。
?
無論是基礎免疫,還是序貫加強免疫,SYS6006都可以持續誘導針對野生株、Delta、Omicron BA.2和BA.5株的特異性T細胞免疫,并在較長時間內維持高水平,且針對不同毒株的細胞免疫強度大致相當。
從安全性而言,SYS6006的安全性較高,各種不良事件發生率較低且程度較輕。且相對于成年組而言,老年組的不良事件發生率及嚴重程度大幅降低,具有更好的風險獲益比,更適合我國的國情。
值得一提的是,該產品是基于石藥集團先進的自主知識產權的工藝技術生產的,更容易實現放大和規模化生產,且產品穩定性較好,可在2-8°C長期貯藏。
?
國內首個新冠mRNA疫苗獲批使用,或許在不久之后,國內多款在研新冠mRNA疫苗也將陸續獲批。
?
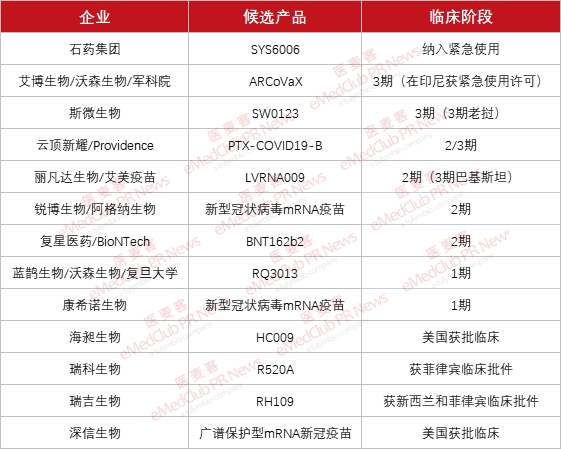
目前,艾博生物/沃森生物/軍科院的ARCoVaX、斯微生物的SW0123、云頂新耀/Providence的PTX-COVID19-B均已經進入臨床后期階段,且國內還有眾多處于臨床階段的企業。想必在未來國內也將會迎來新冠mRNA疫苗獲批的“關鍵期”。
?
參考資料:
1.各企業官網
編輯:小果果,轉載請注明出處:http://www.448371.com/zixun/hydt/27779.html
免責聲明:本站所轉載文章來源于其他平臺,主要目的在于分享行業相關知識,傳遞當前最新資訊。圖片、文章版權均屬于原作者所有,如有侵權,請及時告知,我們會在24小時內刪除相關信息。
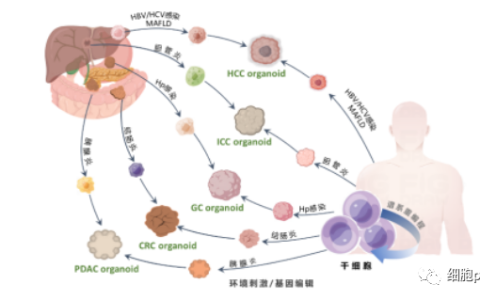
說明:本站所發布的案例均摘錄于文獻,僅用于科普干細胞與再生醫學相關知識,不作為醫療建議。


 微信掃一掃
微信掃一掃  支付寶掃一掃
支付寶掃一掃