介紹
近年來,細胞治療領域取得了顯著進展,包括美國食品和藥物管理局(FDA)批準嵌合抗原受體(CAR) T細胞療法作為治療復發或難治性 CD19+惡性腫瘤包括 B細胞急性淋巴細胞白血病(B-ALL) (1)、彌漫性大B細胞淋巴瘤(DLBCL)(2)和套細胞淋巴瘤(3)。
與T細胞一樣,自然殺傷(NK)細胞是具有強大抗腫瘤能力的免疫效應細胞。然而,與T細胞不同的是,NK細胞不會產生移植物抗宿主病 (GvHD),而且它們的使用也不會導致嚴重的毒性,例如細胞因子釋放綜合征 (CRS) 或免疫效應細胞相關的神經毒性綜合征ICANS(4、5)。
因此,我們假設缺失自我假設(8)所假設的起始信號可以作為通用替代“信號 1”,而共激活受體2B4和4-1BB(11, 12)可以作為“信號 2”。
本文將IL-21R(13)指定為“信號3”的接收器,即細胞因子刺激物,它補充了另一種重要的細胞因子IL-15,IL-15經過基因工程設計用于我們的CAR NK細胞的組成型分泌(9)。因此,我們將CD48、4-1BB 配體和膜結合IL-21 (mbIL-21)設計到基于K562的呈遞細胞上,作為三種信號受體的反配體。這組最小的抗原刺激物形成了我們的通用飼養細胞,用于研究和臨床級非轉導和裝甲CAR NK細胞的穩健擴增,而不管CAR分子靶向的抗原如何。
試驗材料和方法
逆轉錄病毒轉移構建體合成
編碼CD48、CD137 配體 (4-1BBL)和膜結合白細胞介素(IL)-21 (mbIL-21)的逆轉錄病毒載體按規格合成。瞬時逆轉錄病毒上清液的制備如前所述(1)。
用含有CD48、CD137配體和mbIL-21轉基因的逆轉錄病毒上清液連續轉導K562細胞,并在每次轉導后進行有限稀釋克隆以分離特定克隆以進行進一步表征。
編碼抗CD19 CAR的pSFG逆轉錄病毒載體與人類IL15基因和使用2A 序列肽 (iC9.CAR19.CD28-zeta-2A-IL-15)分離的誘導型caspase-9 自殺基因相結合,之前已有描述 (6 , 7) 。
流式細胞術
uAPC用針對IL-21、CD48和4-1BB配體的抗體染色以檢測和量化強制的轉基因表達。
NK細胞分離
健康的人類外周血,通過密度梯度離心分離CB和外周血單核細胞(PBMC)。使用NK分離試劑盒純化CD56陽性NK細胞,并用輻照(100 Gy)uAPC(飼養細胞與NK細胞的比例為2:1)和重組人IL-2在第0天在完全無血清干細胞生長培養基(SCGM)中。
在特定的比較實驗中, uAPC被C9/IL-21取代,C9/IL-21是一種先前表征的飼養細胞,也含有mbIL21。在第+6天,在人纖連蛋白包被的板中用逆轉錄病毒上清液轉導活化的NK細胞。三天后(第+9天),NK細胞再次用照射過的uAPC和IL-2刺激。在第+15天,收集CAR轉導的NK細胞用于指定的測定。
NK細胞表型分析和功能分析
在離體培養的14-21天內評估NK細胞生長,并每3天使用臺盼藍排除法計算存活率。通過FACS評估NK細胞的CD48、IL-21、CD137L(4-1BBL)、CD14、CD45和CD32(以識別K562)的表達。CAR轉導的CB-NK細胞用Alexa-Fluor647親和純化的F (ab’)2片段山羊抗人IgG (H+L)抗體CAR Ab染色CAR表達。
此外,還在培養的第14天使用離體擴增的非轉導(NT)和iC9/CAR.19/IL-15 (CAR) NK細胞測量細胞內細胞因子。為了評估效應子功能,將NK細胞以 0.25×106個細胞/孔在96孔板中與Raji細胞或 K562 靶標(陽性對照)以效應子與腫瘤細胞的比率(E:T 比率)5:1共培養5小時。CD107a脫粒和細胞內細胞因子產生的測量如前所述(11)。
NK細胞細胞毒性試驗
為了評估細胞毒性,將體外擴展研究或良好生產規范(GMP)級NT和 iC9/CAR.19/IL-15(CAR)轉導的NK細胞與51Cr標記的Raji和K562靶標(陽性控制)在不同的E:T比率。通過51Cr的釋放來測量細胞毒性。
小鼠異種移植模型
我們使用NOD/SCID IL-2Rγ無效(NSG)異種移植模型(9)和侵襲性NK抗性Raji 細胞系,評估CAR轉導的CB-NK細胞的體內抗腫瘤作用。成年NSG小鼠(10-12周大)在第0天接受300cGyγ輻射,并在第0天靜脈內接種用螢火蟲熒光素酶(ffluc)轉基因穩定轉導的 Raji 細胞(2×104)。使用uAPC或C9/IL-21作為飼養細胞的新鮮擴增的CAR轉導的CB-NK細胞,然后在第0天以3×106個細胞的劑量在200μL體積中通過尾靜脈注射。小鼠每周接受一次生物發光成像。
RNA測序(RNA-Seq)
在第0天(基線)或擴增后15天,從 5×106 離體擴增的NT和iC9/CAR.19/IL-15 (CAR) 純化的NK細胞中提取和純化RNA uAPC。SmartSeq2 RNA-seq文庫如(13)所述制備。使用Illumina HiSeq 2500 (16)合并索引文庫并使用50 bp雙端讀取進行測序。
質譜流式細胞術
簡而言之,在MD Anderson Cancer Center Flow and Mass Cytometry Core Facility使用來自Fluidigm的 MaxPar抗體標記試劑盒(目錄#201300)用金屬標簽標記抗體。校準珠被門控,并根據銥193染色和事件長度選擇單線態。死細胞被 Pt195通道排除,并進行進一步的門控以選擇CD45+細胞,然后選擇感興趣的NK 細胞群(CD3-CD56+)。t-SNE分析是使用自動降維進行的,包括(viSNE)與FlowSOM結合用于靜息NK細胞(未刺激,第0天)的聚類或與uAPC共培養14天(擴增的NK細胞)。
uAPC合規性驗證和GMP使用
驗證計劃和程序是根據FDA指南(18, 19)制定的,以符合人類基因治療研究新藥申請(IND)的化學、制造和控制(CMC)信息要求,并控制關鍵過程,控制電池產品的安裝、操作和性能資格(20)。通用和產品特定的特性以及階段特定的要求都得到了保留。過程中和最終產品測試包括:無菌、內毒素、支原體(細胞收獲時的PCR 測試)、活力、鑒別(通過流式細胞術識別特定細胞類型)和體外功能性殺傷。
使用uAPC進行GMP NK細胞擴增
使用G-Rex?生物反應器(美國明尼蘇達州圣保羅)與uAPC共培養擴增NK細胞,用于CB-NK CAR臨床試驗(21)(NCT 編號:NCT03056339)。這種封閉的細胞培養系統可以使用帶有透氣膜的燒瓶,從而實現最佳的氣體交換并確保有氧生長動力學。使用先前優化的變量,包括細胞接種密度、校準的培養基體積和培養基配方,我們能夠從臨床前協議中調整G-Rex M100系列,以在GMP設置中將程序轉換和線性縮放到所需的產量。
端粒長度分析
CB-NK細胞中的端粒長度使用絕對人端粒長度定量qPCR檢測試劑盒并按照制造商的說明通過定量PCR進行檢測。
統計分析
均值標準誤(SEM)用于比較CB NK細胞倍數擴增和效應子功能的差異。統計顯著性確定為 p≤0.05。
試驗結果
逆轉錄病毒轉導共表達4-1BBL、CD48和膜結合IL-21的基于K562的飼養細胞的生成和優化
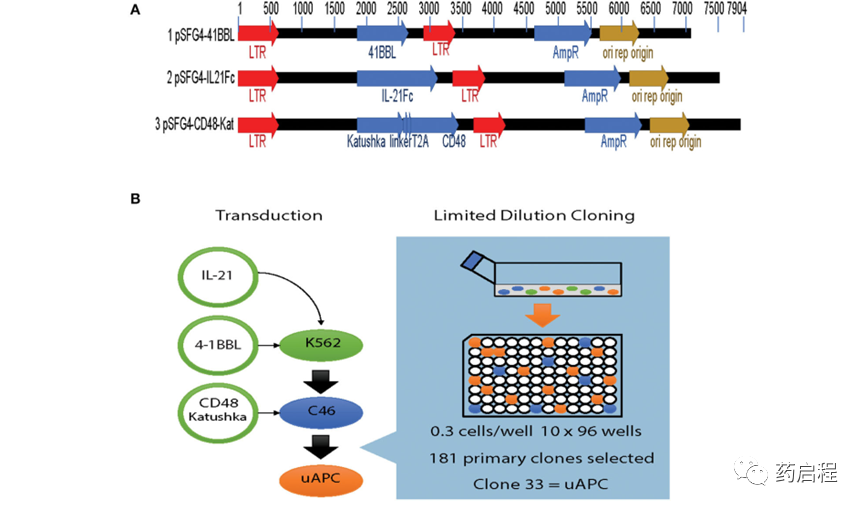
圖 1. 基于K562的通用抗原呈遞細胞 (uAPC) 的生成。
使用流式細胞術門控策略對親本 K562、克隆 46 和 uAPC 細胞進行免疫表型分析,如圖 2A 所示。簡而言之,選擇“髓樣”門控細胞作為單細胞,并研究活細胞的 mbIL-21、4-1BBL(CD137L)和 CD48 表達(圖 2B-D)。uAPC 中的 mbIL-21、4-1BBL 和 CD48 轉導效率 >75%,并且在 300 天內保持穩定(圖 2E)。CD32 用于確認 K562 細胞的身份。因此,這些數據證實了穩定共表達 mbIL-21、4-1BBL 和 CD48 的基于 K562 的 uAPC 細胞系的產生。我們還證實,我們基于基因工程 K562 的 uAPC 的倍增時間范圍為 23.26 至 26.42 小時(n = 3 個獨立實驗),這與之前關于親本 K562 和衍生細胞系的報告一致 (10)。
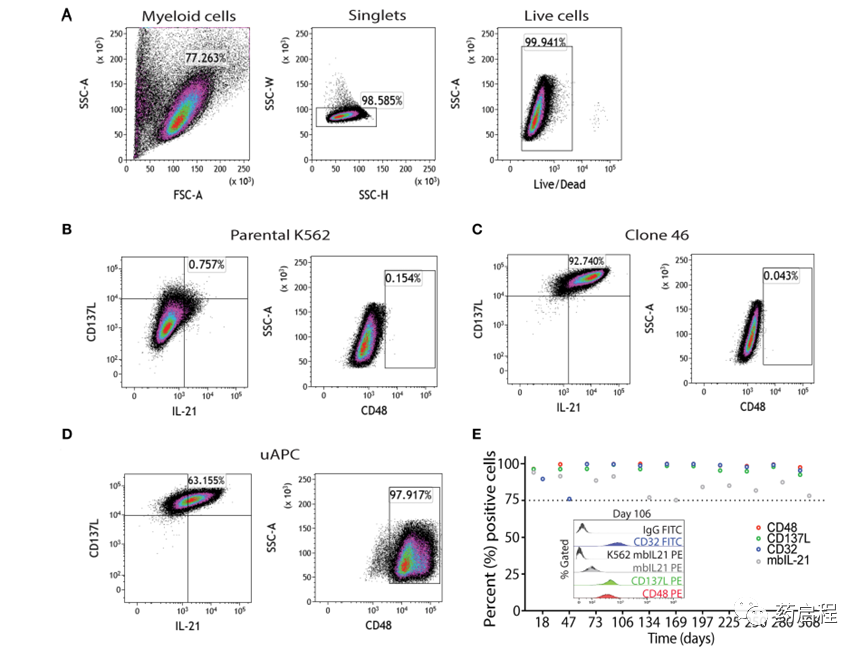
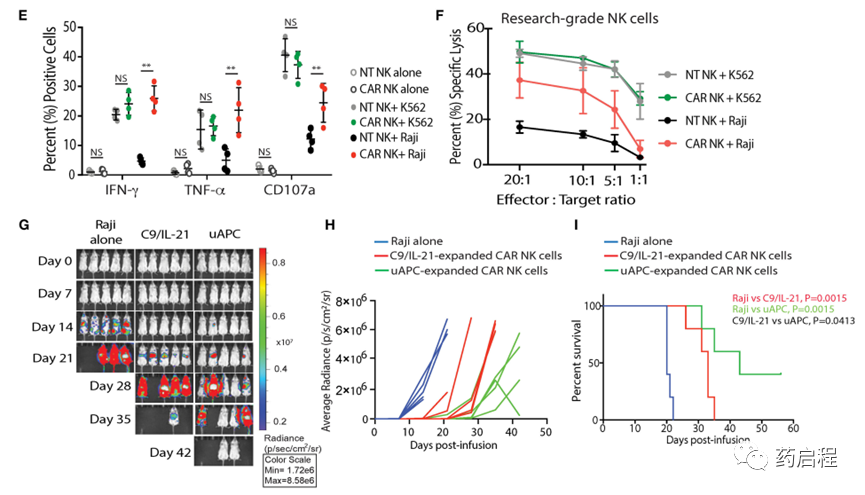
圖 2. uAPC 的表型特征。
uAPC增強研究級裝甲CAR-NK細胞的抗腫瘤活性
首先,我們測試了uAPC是否可以促進CB-NK細胞的體外擴增。在與uAPC共培養7天和14天后,我們觀察到研究級NK細胞的9倍(中值=8.96,范圍=8.26-10.1)和 903 倍擴增(中值=784,范圍=752-1,174)(圖 3A)。
重要的是,與uAPC共培養的非轉導(NT)對照和iC9/CAR.19/IL-15(CAR轉導)研究級NK細胞在第15天和第22天均表現出高NK細胞純度(>97%)。通過流式細胞術確定與uAPC共培養(圖 3B、C)。
此外,uAPC擴增的iC9/CAR.19/IL-15 (CAR)-NK細胞保留了它們的CAR表達(>85%)(圖 3B、C),產生顯著更高水平的IFN-γ和TNF-α,并顯示與NT NK 細胞相比,對CD19+ Raji淋巴瘤細胞的更多脫顆粒(CD107a)和細胞毒性(圖 3D-F)。CAR NK細胞在殺死CD19陰性K562靶標方面與NT NK細胞一樣有效(圖 3F),表明先天NK細胞殺傷機制在uAPC刺激后保持不變。我們還測試了uAPC支持NK細胞擴增超過14天的能力。NK細胞用uAPC+IL-2擴增1周。然后在每周存在或不存在每周uAPC飼養細胞的情況下收集細胞并與IL-2 (100 U/ml)一起長期培養。

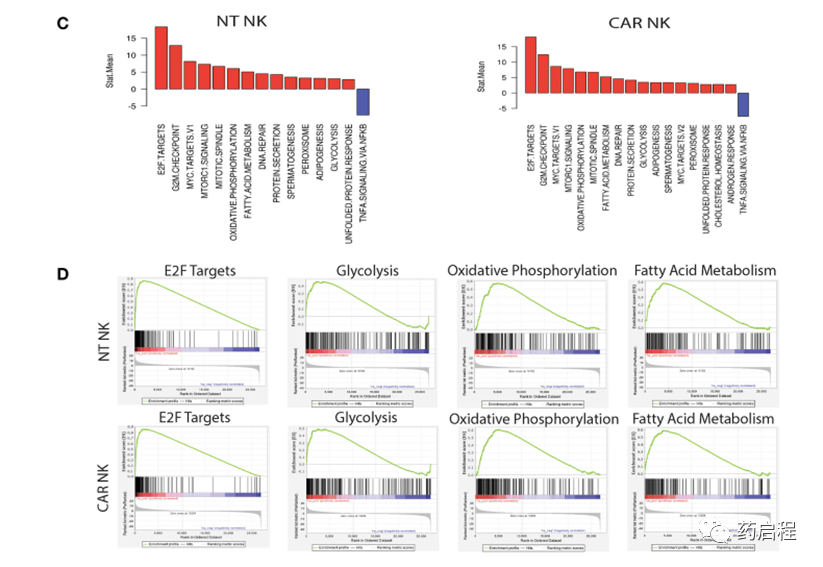
圖 3. uAPC 促進研究級 NT 和 iC9/CAR19/IL-15 NK 細胞的增殖和細胞毒性。
此外,我們比較了用uAPC擴增的CAR轉導的CB-NK細胞的端粒長度、體外和體內活性與先前報道的表達4-1BBL和mbIL21的K562衍生的APC (C9/IL-21) (15)。我們觀察到在體外使用兩種飼養細胞系產生的NK細胞的端粒長度(補充圖 3)、倍數擴增或細胞毒性沒有顯著差異。重要的是,uAPC擴增的CAR-NK細胞在Raji異種移植小鼠模型中發揮了優異的體內抗腫瘤活性(圖 3G-I)。在直接比較中,使用由同一CB供體產生的CAR-NK細胞,接受用uAPC擴增的CAR-NK細胞的小鼠實現了更好的腫瘤控制(圖 3G、H)并且與用CAR治療的動物相比存活時間明顯更長(圖 3I) – 用 C9/IL-21生成的NK細胞。總之,這些數據支持這樣一種觀點,即NK細胞激活的三信號模型能夠使NK細胞穩健擴增并具有更強的抗腫瘤效力。
?
與uAPC刺激相關的NK細胞表型和分子特征
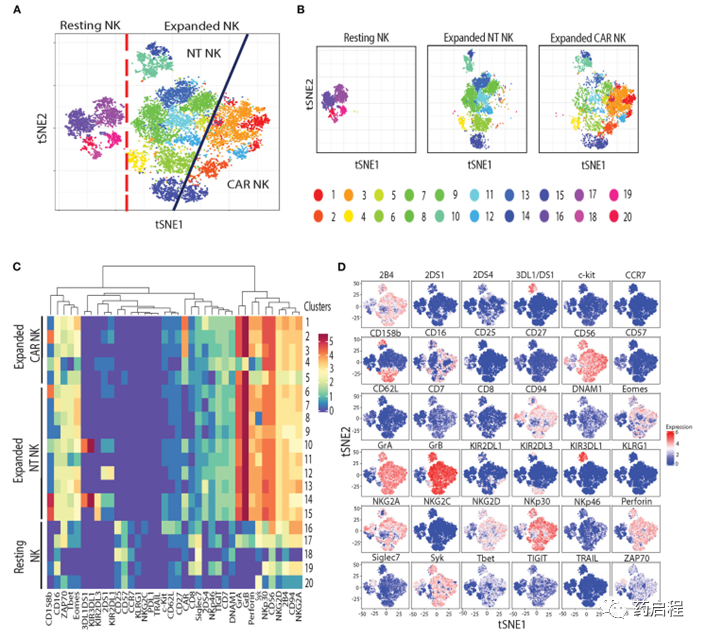
圖 4. uAPC 擴增的 NT 和 iC9/CAR19/IL-15 NK 細胞的分子特征。
暴露于uAPC(第15天)后NT和CAR NK細胞的轉錄組學分析顯示,與基線(第0天)相比,與效應子功能相關的基因上調。重要的是,我們沒有觀察到任何與疲勞、無反應性或衰老相關的途徑(圖 4B)。在uAPC刺激的NT和CAR NK細胞中,與細胞周期、細胞膜形態和代謝途徑相關的基因同樣增加(圖 4C)。基因集富集分析(GSEA)揭示了uAPC激活的NT和CAR NK細胞中涉及 E2F 靶標、糖酵解、氧化磷酸化和脂肪酸代謝的基因的富集(圖 4D)。特別值得注意的是,這些代謝動員模式與脂質生物發生和細胞膜重組相一致,表明了一個活躍的程序,表明細胞增殖以及NK細胞內效應器成分的啟動以準備細胞毒性活動(24)。二維主成分分析 (PCA)的特征值截止值為1和2,可以通過其不同的狀態輕松區分樣品(補充圖 6),進一步支持我們擴增的NK細胞的非克隆性質。
接下來,為了評估與NK細胞中uAPC擴增相關的表型變化,我們使用了飛行時間(CyToF)細胞術和一組36種針對抑制性和激活性受體的抗體,以及分化、歸巢和激活標記物。我們鑒定了20個不同的NK細胞簇,它們表征靜息、uAPC擴增的 NT和CAR NK細胞(圖 5A、B)。
靜息NK細胞主要由16-20簇組成,而簇 1-5 僅在擴增的CAR NK細胞中觀察到,簇6-15由擴增的NT和CAR NK細胞共享(圖 5A、B)。uAPC擴增的NT和CAR NK細胞均顯示出激活和細胞毒性標志物的表達增加,包括顆粒酶A (GrA)、顆粒酶 B (GrB)、穿孔素;與靜息NK細胞相比,轉錄因子(Eomes、T-bet)和激活受體(NKp30、NKG2D、2B4、CD94/NKG2C)(圖 5C、D)。總之,這些數據表明uAPC培養增強了NT和CAR NK細胞的活化和抗腫瘤活性,同時保留了它們的CAR特異性。
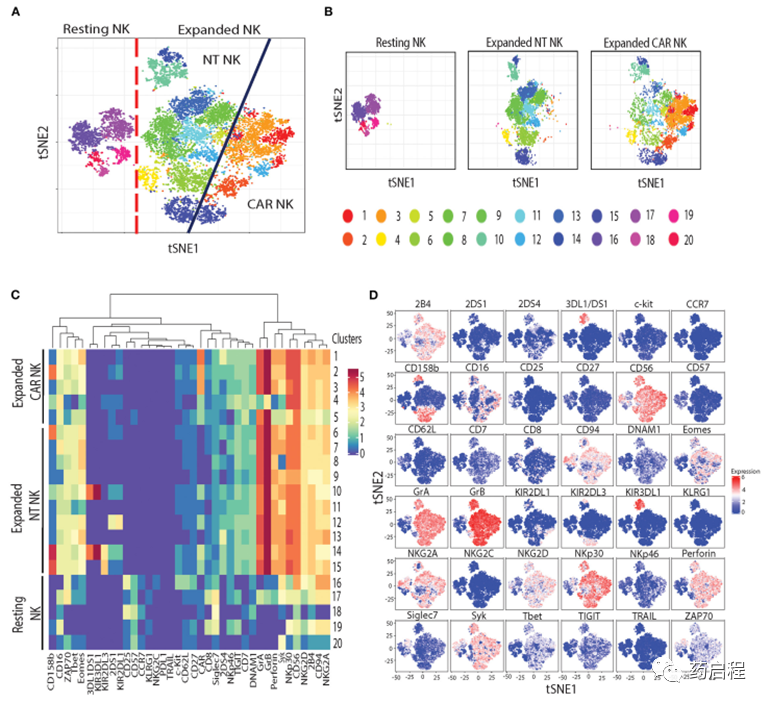
圖 5. 靜息與 uAPC 擴增 NK 細胞的表型特征。
用于cGMP的臨床級uAPC的驗證和表征
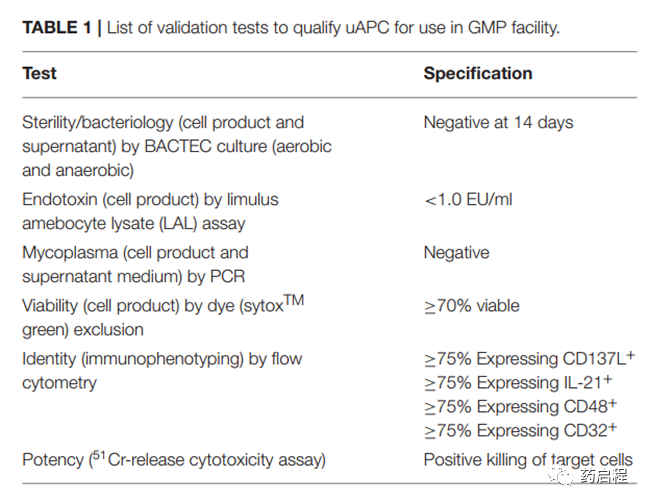
為了在cGMP環境中使用uAPC來生成基于NK細胞的治療產品,我們根據當前的最佳實踐基于發布標準進行了一系列驗證運行。我們建立并分析了表 1 中列出的釋放標準,包括無菌性、活力、特性和效力,如所示滿足監管要求。此外,還建立了處理和使用uAPC以促進NK體外擴增用于臨床生產的標準操作程序,以幫助質量保證和質量控制。作為我們確保uAPC在臨床使用中的完整性的努力的一部分,我們還對uAPC進行了遺傳指紋識別,并表明STR譜與K562親本譜系相匹配。?
在制定和建立GMP級uAPC的發布標準后,我們在GMP實驗室驗證和表征了NK細胞擴增過程。與在使用前按需生長和輻照的研究級uAPC批次相比,臨床級uAPC批次會根據需要進行膨脹、輻照、冷凍保存和解凍以備使用。與研究級 CB NK細胞(圖 3A)類似,GMP級CB NK細胞產品在與GMP級uAPC共培養后第14天和第21天顯示出強勁的擴增(>1,000 倍)(圖 6A)。重要的是,用GMP級uAPC 擴增的NT和 iC9/CAR.19/IL-15 (CAR) NK細胞具有出色的純度,檢測到低頻率至零T細胞(0.01-0.04%)(圖 6B、C)。在我們的臨床NK細胞產品中,低T細胞污染是預防 GvHD 的必要條件。此外,擴增的細胞群是CD45+CD32-,表明沒有uAPC細胞生長(圖 6B、C)。與NT對照相比,使用GMP級uAPC刺激的iC9/CAR.19/IL-15 (CAR) NK細胞對Raji淋巴瘤細胞發揮更大的細胞毒性(圖 6D),而uAPC刺激的NT和 iC9/CAR.19/IL -15 (CAR) NK細胞在殺死K562靶標方面同樣有效(圖 6D)。一旦臨床級uAPC在GMP實驗室得到驗證,就建立了一個主細胞庫,并在正在進行的I/II期臨床試驗中為我們獲得了FDA的批準。
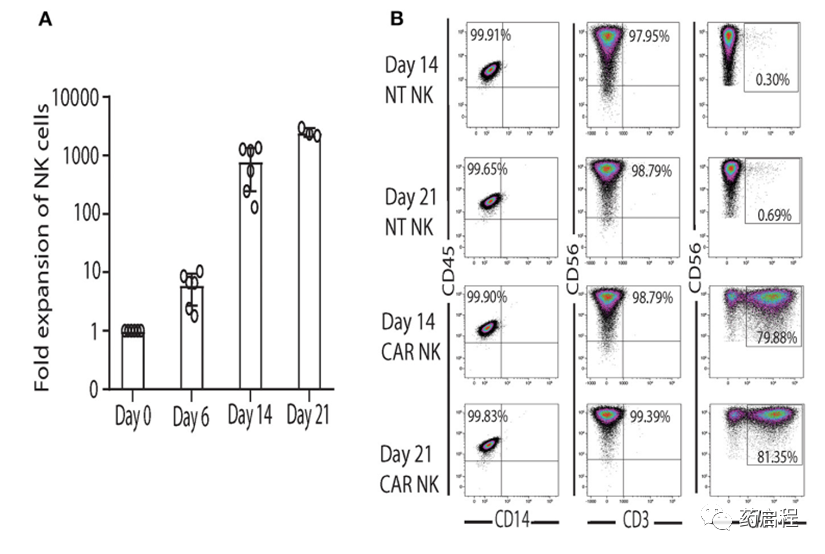
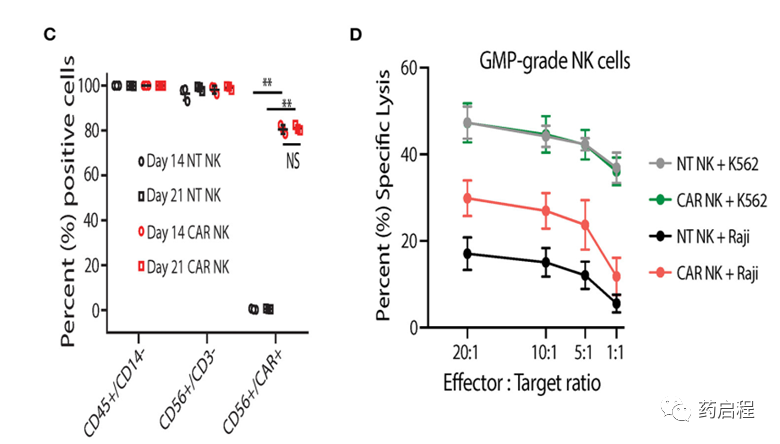
圖 6. 與GMP級uAPC共培養的臨床級NK細胞顯示出強大的擴增和抗腫瘤活性。
討論
在未經處理的臍帶血或外周血單核細胞部分中發現的NK細胞數量相對較少,限制了NK細胞免疫療法的治療應用。因此,NK細胞的體外擴增已越來越多地用于產生臨床相關劑量。
跨膜4-1BB是目前最常用的共刺激受體,可與CD80/86以及IL-2、IL-15和IL-21 的各種組合一起擴增NK細胞。我們的方法利用獨特的SLAMF介導的NK細胞免疫雕刻來優化臨床應用的產品。
我們的目標是確定一組最小的抗原刺激,足以在2-3周內觸發研究和臨床級NK細胞的最佳體外擴增。選擇K562腫瘤細胞系作為刺激細胞,因為它們(1)大部分缺乏MHC決定簇,因此對NK細胞的細胞毒性敏感,(2)在懸浮培養中生長,易于與NK 細胞的相互作用,(3)具有相對18-24小時的短倍增時間和(4)很容易且穩定地被逆轉錄病毒轉導,以根據需要強制表達抗原。
NK細胞中的“信號1”(39)沒有已知或簡單的替代品(例如T細胞中的TCR-MHC 相互作用)。NK細胞和靶細胞之間直接物理相互作用的啟動極大地影響了NK細胞在殺死或保留靶細胞方面的反應。因此,我們建議由KIR識別uAPC上HLA I類缺失介導的“失蹤自我”相互作用是NK細胞中“信號 1”反應的最接近替代物。為了誘導信號 2(輔助受體)引發的細胞相互作用,我們考慮使用來自同源免疫球蛋白受體的信號淋巴細胞激活分子(SLAM,以前也稱為CD2超家族)的抗原,這些受體廣泛表達并在免疫系統中發揮關鍵作用,具有細胞間相互作用的一個特別重要的特征。我們使用CD48作為uAPC中的替代“信號 2”來啟動與NK細胞的細胞間相互作用。CD48 是一種存在于細胞表面的糖基磷脂酰肌醇錨定蛋白(GPI-AP),參與免疫細胞的粘附和激活途徑。盡管缺乏細胞內結構域,CD48的刺激會誘導脂筏中信號因子的重排、Lck激酶活性和酪氨酸磷酸化。作為粘附和共刺激分子,CD48是2B4的反受體,2B4是NK細胞的重要激活劑(40)。
我們還使用4-1BB配體作為第二個“信號 2”來介導 NK 細胞增殖和分化。值得注意的是,4-1BB在我們在第15天收集uAPC刺激的 NK 細胞中顯著上調(圖 4A)。在活化的 NK 細胞中,CD137 是一種細胞因子誘導型共刺激分子,它反過來通過增加細胞增殖和 IFN-γ 分泌來驅動 NK 細胞的抗腫瘤反應。使用 CD137L-/- 基因敲除小鼠的研究表明 CD137/CD137L 信號軸在抗腫瘤免疫細胞發育中的重要性。CD137 在調節 NK 細胞介導的抗腫瘤作用中的關鍵作用在 CD137-/- 基因敲除小鼠中很明顯,與對照小鼠相比,這些小鼠的腫瘤轉移頻率高 4 倍。4-1BB 配體(4-1BBL、CD137L)形成同源三聚體胞外域,具有獨特的三葉螺旋槳構象 (41),不同于腫瘤壞死因子 (TNF) 超家族其他成員形成的三聚體,暗示功能性分子信號的差異 (42)。雖然可以用抗4-1BB抗體刺激NK細胞上的4-1BB,但我們選擇了4-1BB 配體 (41BBL),CD137的生理反受體,以獲得最佳刺激。
細胞因子信號傳導對于維持淋巴細胞存活、增殖和效應器功效也至關重要。體內IL-2給藥?FDA批準的用于在患者體內擴增免疫細胞的唯一方法。認識到細胞因子刺激對 NK細胞健康的重要性,我們的“信號 3”策略是將mbIL-21封裝為 uAPC 的一部分。對于基因工程化以表達CAR的NK細胞,我們編碼了一個用于組成型自分泌分泌的IL-15表達盒 (9)。
雖然我們注意到與uAPC孵育后NT和CAR NK細胞中IL-21R(圖 4A)的下調,但這種觀察的機制仍有待確定。能量學(糖酵解、氧化磷酸化和脂肪酸代謝)和脂質生物發生基因的動員符合增殖NK細胞的代謝特征(44)。重要的是,缺乏與衰竭、無反應或衰老相關的生物標志物(圖 4B)支持我們生產準備靶向癌癥的NK細胞的目標。此外,通過質譜流式細胞術對NK細胞的表型分析(圖 5)產生了獨特的靜息和激活 NK 細胞群,表明非克隆擴增。
總之,我們的適應性強且強大的 uAPC 平臺不是僅僅依賴商業供應商提供關鍵生物試劑,這可能導致不可預測和有害的供應鏈中斷,而是在一個緊湊的包裝中提供必要和預期的 NK 細胞刺激,以供持續臨床使用。


D
O
i
:
GMP-Compliant Universal Antigen Presenting Cells (uAPC) Promote the Metabolic Fitness and Antitumor Activity of Armored Cord Blood CAR-NK Cells
doi: 10.3389/fimmu.2021.626098
編輯:小果果,轉載請注明出處:http://www.448371.com/linchuang/lcyj/9275.html
免責聲明:本站所轉載文章來源于其他平臺,主要目的在于分享行業相關知識,傳遞當前最新資訊。圖片、文章版權均屬于原作者所有,如有侵權,請及時告知,我們會在24小時內刪除相關信息。
說明:本站所發布的案例均摘錄于文獻,僅用于科普干細胞與再生醫學相關知識,不作為醫療建議。


 微信掃一掃
微信掃一掃  支付寶掃一掃
支付寶掃一掃