?
● ? ?● ? ? ●
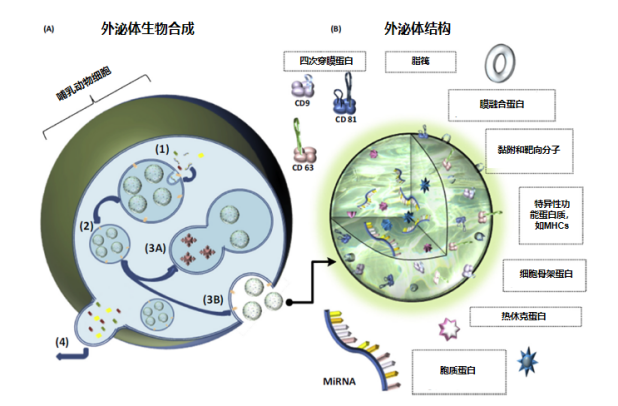
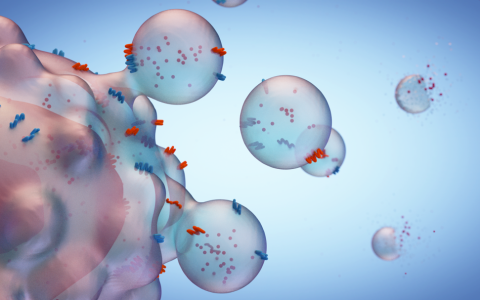
圖 1?外泌體的生物來源過程和結構
–01–
外泌體的概念

圖 2?外泌體從核內體和質膜中萌發
–02–
外泌體的提取
所有的細胞都可以分泌外泌體,機體的體液內和間質中均含有大量的外泌體。由于生物體內所含有的細胞或者蛋白非常豐富,因此從體內提取外泌體是非常困難的,而且外泌體來源的細胞也無法確定。
?
近年來,來自干細胞的外泌體引起了科學家們的關注。干細胞具有特殊的分化潛能,因此在醫用再生領域被廣泛研究,并應用于不同的組織修復和再生中。而近期科學家們發現,干細胞在組織再生中,相較于其自身的分化潛能,可能更多是通過旁分泌作用調控了組織微環境以及其他細胞的行為。其分泌的外泌體,正是非常重要交流介質,起到干細胞與其他細胞之間的溝通交流。于是,科學家們在實驗室培養大量的干細胞,進而提純并收集外泌體,再研究其在組織修復以及疾病中的應用。
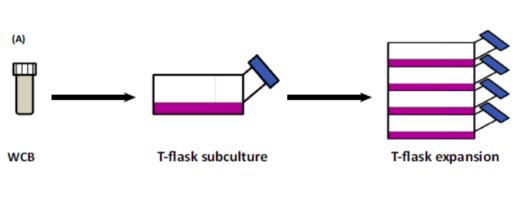
現如今有兩類廣泛使用的用于提純外泌體的方法:超速離心法和Thermo Fisher等公司生產的提純試劑盒。
?
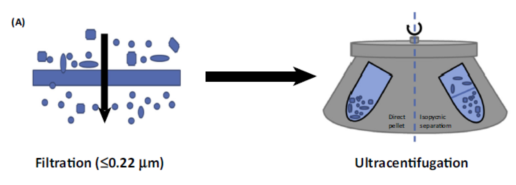
超速離心法,主要是通過將實驗室培養干細胞所得到的培養基通過濾膜濾掉尺寸較大的細胞碎片及細胞外囊泡后,通過超速離心機在100,000g的離心力的作用下富集得到外泌體。
?
提純試劑盒,主要是通過試劑包被外泌體,使其尺寸和重量增大,從而在10,000g的離心力即可得到外泌體。試劑盒的使用有導致外泌體污染的風險,在科研領域超速離心法更為常見。
–03–
外泌體的生物學特性
由于外泌體在再生醫美領域顯示出極大前景,這也迎來產業化合作的新浪潮,眼下外泌體似乎已經成為下一個生物醫藥的黃金賽道。科學家們普遍認為,外泌體具有其獨特的生物學特征,可以反映來源細胞的表型。
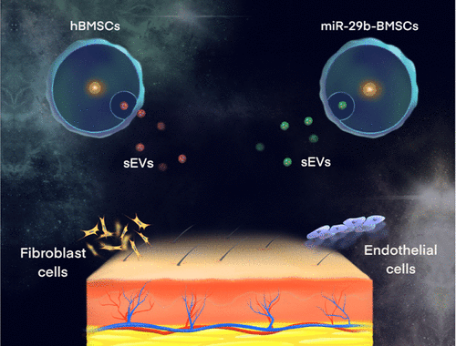
圖 5?外泌體促進皮膚修復
不同細胞分泌不同的外泌體,因此外泌體的應用是多種多樣的。一方面,外泌體被認為是多種癌癥的疾病診斷生物標志物。外泌體獨特的miRNA譜圖和疾病載體作用,使得其頻繁出現在卵巢癌、膠質母細胞瘤、黑色素瘤、前列腺癌和結腸癌。另一方面,外泌體也可以作為細胞信號傳導的有效媒介而廣泛用于醫學再生領域。例如,它們能夠將RNA和蛋白質的信息從來源細胞轉移到周圍環境中的其他細胞。實驗證明,來自小鼠胚胎干細胞的外泌體在體外促進了小鼠造血干細胞的存活和擴展,同時也上調了受體細胞中與多能性相關的轉錄因子。干細胞來源的外泌體與生物材料相結合,促進骨組織以及關節軟骨的修復和再生。
?
在皮膚組織再生中,外泌體的應用尤其廣泛。如脂肪源外泌體能通過減少IFN-α的分泌而發揮免疫抑制作用,從而抑制T細胞的激活。此外,外泌體含有免疫調節蛋白如TNF-α、巨噬細胞集落刺激因子(MCSF),從而通過良好的炎癥調節保證了傷口愈合。而在皮膚愈合過程中,外泌體則能通過優化成纖維細胞特性加速皮膚傷口愈合。在一項研究中發現,外泌體上調199個miRNA,下調93個miRNA,促進真皮成纖維細胞增殖和分化,加速皮膚再生。
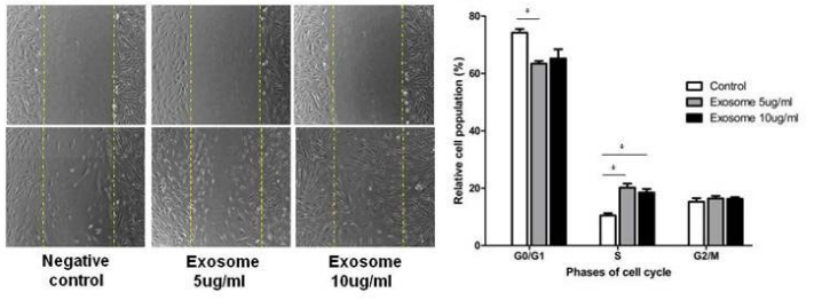
圖 6?外泌體促進皮膚細胞增殖
總而言之,干細胞來源的外泌體作用廣泛。在皮膚再生中,外泌體可以通過調控炎癥、促進皮膚修復等多方面提供作用;在疾病發展中,外泌體也參與多種病理通路。在未來,無論是組織再生、皮膚修復、還是疾病研究,外泌體都將在其中扮演重要角色。
–04–
外泌體的缺陷
外泌體具有諸多優點,在醫用再生中具有難以忽視的價值。然而,外泌體的應用卻還有所局限。
?
最適用于提純外泌體的超速離心法,在提純得到外泌體的過程中會導致大量的外泌體損失,至少80%的外泌體會因為收集的損失或者在超離過程中其獨特的磷脂雙分子層的膜破碎而無法維持其正常形態。
此外,外泌體在提純后其保存比較困難,需要保存的試劑具有與體液類似的滲透壓從而維持其磷脂雙分子層的膜結構,否則其內含的具有生物功能的蛋白質和miRNAs也容易失去活性。另外,外泌體起到信號傳導作用,但本身并不會提供結構支持。因此,在修復領域,外泌體難以單獨使用。
?
?
–05–
細胞外基質:外泌體的最佳搭檔
所有細胞均可分泌外泌體,外泌體充當著細胞之間信息交流的介質,因此外泌體生理功能的實現是通過一個細胞“出”而“進”入到另一個細胞內。在組織內部,必然要穿越細胞外基質。
?
因此,外泌體更適合作為細胞外基質的一部分來發揮價值,而細胞外基質的獨特生理結構和生理穩態一來可以幫助維持外泌體的活性、二來也能與外泌體協同作用,實現更好的修復和再生效果。

在醫用再生領域,科學家們研究各種各樣的生物材料,并與外泌體進行復合促進組織的修復和新生。細胞外基質無疑是最安全的并且可以與外泌體協同發揮作用的生物材料。細胞外基質本身即源于人體,具有多元的組成(膠原蛋白、彈性蛋白、層黏連蛋白等等)。
?
一方面,細胞外基質能夠起到結構支持作用,作為承載材料提供組織再生的根基;另一方面,細胞外基質中復雜的結構和靶點可以維持外泌體的活性,從而高效發揮外泌體的性能。外泌體可以通過進入細胞內發揮其優異的生物學功能,?而細胞外基質作為載體即可以為細胞的黏附和遷移提供平臺。如果沒有細胞外基質所提供的平臺,那么外泌體會很快隨著體內的生理循環和代謝而流失,從而失去了其作用效果。眾所周知,外泌體價格昂貴。當外泌體由細胞外基質承載、由細胞外基質保護時,才會更好地提高其生物利用度,取得更好的修復效果。
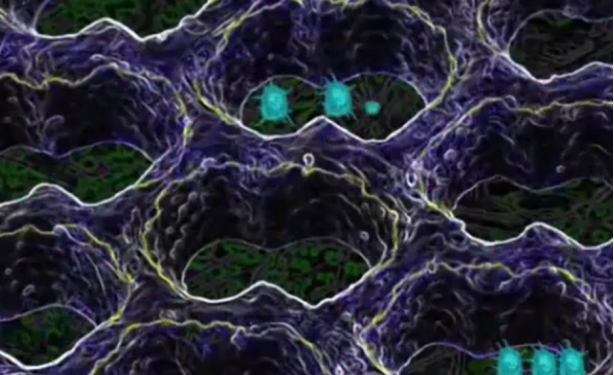

組織修復和再生,與細胞微環境息息相關。簡單來說,微環境由兩個基本組成部分組成,一個是細胞外基質(ECM),而另一個是細胞分泌的外泌體、生長因子等功能性物質。二者缺一不可,彼此相輔相成、緊密結合。因此,光有外泌體,沒有細胞外基質是遠遠不行的。
?
其實,除去細胞外基質對外泌體的負載和保護作用,其本身也具備出眾的再生和修復能力。除了提供細胞存在的平臺,細胞外基質的多元組成既可以為細胞的生理活動提供養分,并駐留在原位,成為機體自身的細胞外基質的一部分;又能夠通過其本身的生物學特性來協同外泌體,實現更好的修復和再生效果。在經典的修復再生過程中,細胞外基質可以調節干細胞的表型和表達,而外泌體則含有控制干細胞分化的表型特異性指導因子(miRNA,RNA和蛋白質)。
圖 8?皮膚修復與再生
簡而言之,細胞外基質可以從拓撲結構、生物力學、功能靶點等多個維度與外泌體、生物因子共同作用,從而形成適于組織修復的胞外微環境。
?
首先,細胞外基質所含有的多種蛋白、多糖成分構建出其獨特的三維結構和表面拓撲學特征。除支撐組織的生理形態外,還能夠調控募集細胞的黏附、增殖和分化行為。近年來,人們更是發現細胞外基質構建的拓撲學結構與免疫細胞的免疫應答等行為息息相關,進而調控組織再生。
?
再者,細胞外基質本身具有其獨特的生物力學性質。不同彈性模量、不同硬度的基質,能夠引發細胞的不同表現行為和分化方向,也會引起細胞分泌和募集因子的不同。
?
細胞外基質極為多元的組成能提供不同的生物學效果,從而建立修復微環境。舉例來說,細胞外基質中的纖連蛋白因可與細胞表面的整合素蛋白的α5β1結合,充當修復過程中細胞與細胞外基質交流溝通的重要參與者,并且調控細胞的黏附、增殖、形態和分化等行為;蛋白聚糖通過參與調節細胞外基質的組裝和維持,并通過與生長因子的相互作用參與細胞增殖等細胞行為,在組織的生理和生物力學功能中發揮重要作用。正是由于細胞外基質打下的堅實基礎,才能讓外泌體、細胞因子等活性成分進一步“錦上添花”。
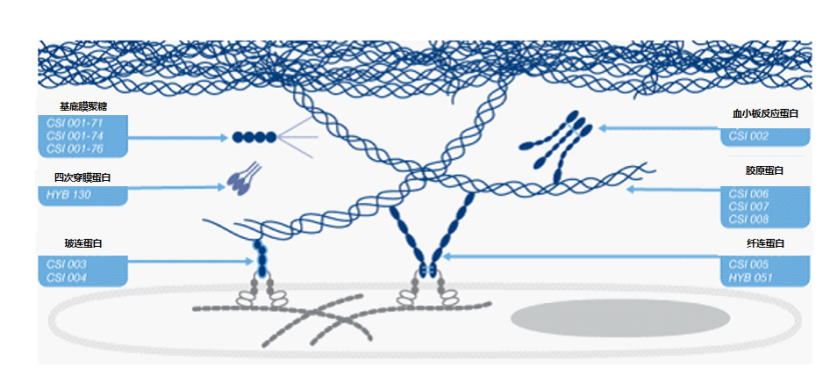 圖?9?細胞外基質多作用靶點
圖?9?細胞外基質多作用靶點另外,近幾年研究中還發現,細胞外基質的結構能結合和錨定多種生長因子(如VEGF,HGF等)、多肽短鏈。一方面,通過構型調整來更好地發揮其生物活性;另一方面,則能形成生長因子梯度,從而介導修復和再生過程的進行。可以想象,這是唯有細胞外基質才能實現的高度復雜而有序的生物過程。相比之下,僅僅使用外泌體完全無法實現上述空間上的介導過程。這也解釋了為何直接使用外泌體或生長因子時,往往修復和再生效果并不如人所愿。
?
關于細胞外基質和外泌體之間的作用,目前依然還在不斷研究中。然而,我們已經可以知道的是:細胞外基質是組織再生的舞臺,而外泌體則是舞臺上的演員。演員可以讓舞臺更加熠熠生輝,但舞臺卻是整個根基所在。二者有機結合,則能帶來最好的演出效果。
?
–06–
細胞外基質/外泌體組合的應用
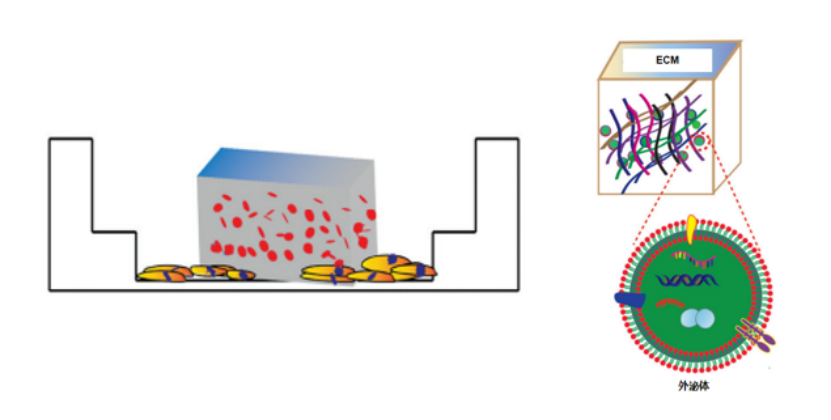
圖 10?負載外泌體的ECM再生材料
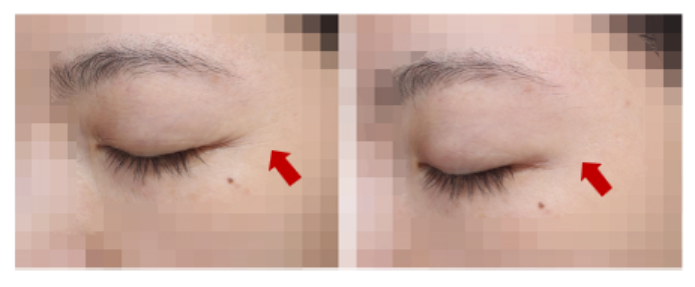
圖 11?細胞外基質/外泌體組合在皮膚年輕化中的應用
?
–07–
文末小結
隨著技術的進步,外泌體已經越來越被人們熟知,其應用也愈加廣泛。外泌體是具有納米尺寸的細胞囊泡,具有高生物活性,能參與細胞之間的交流,調控炎癥水平、促進組織再生。然而,外泌體提取較為困難,本身也不具備結構性的功能,因此單獨使用有所局限。
?
作為細胞外基質中的一部分,當外泌體回到細胞外基質中時,能夠發揮出更為強大的作用,更起到“錦上添花”的效果。細胞外基質一方面是外泌體最理想的載體,幫助維持外泌體的活性;另一方面細胞外基質能夠構建出最適宜再生的細胞外微環境,從而讓外泌體能更加有的放矢。
?
目前,國內外相關的研究正如火如荼地進行中。相信,不久的將來,細胞外基質/外泌體這樣的明星組合會越來越多地出現在我們面前。

相關鏈接
—? END ?—?
編輯:小果果,轉載請注明出處:http://www.448371.com/cells/wmt/8746.html
免責聲明:本站所轉載文章來源于其他平臺,主要目的在于分享行業相關知識,傳遞當前最新資訊。圖片、文章版權均屬于原作者所有,如有侵權,請及時告知,我們會在24小時內刪除相關信息。
說明:本站所發布的案例均摘錄于文獻,僅用于科普干細胞與再生醫學相關知識,不作為醫療建議。


 微信掃一掃
微信掃一掃  支付寶掃一掃
支付寶掃一掃