最近幾個月,CAR-T 領域出現了一些重大的飛躍。這些前所未有的成功故事表明,通過我們不斷增強的改造 T 細胞的能力,我們很可能會對多種傳統療法不起作用或沒有可用療法的疾病產生重大突破。CAR-T 可被視為典型的個體化藥物,其通過使用基因工程化手段對 T 細胞進行改造,使它們能夠識別人體細胞表面的特定蛋白質抗原,從而顯著提高或降低它們的免疫反應。
正如本周《Science》雜志所評論的那樣,目前有超過 500個臨床試驗正在進行當中,這些試驗是在2017年首次批準的第一代嵌合抗原受體 (CAR-T) 細胞治療白血病的基礎上,測試通過新的工程化手段改造的 T 細胞。目前,已有超過2萬人接受了獲得 FDA 批準的 6種 CAR-T 產品中一種用于治療所謂“液體性的”血液癌癥。Carl June 團隊最近報道,12年前第一批接受 CAR-T 治療的癌癥患者中,有兩名試驗者目前仍處于緩解期,CAR-T 仍然在其體內控制癌細胞的再度出現。

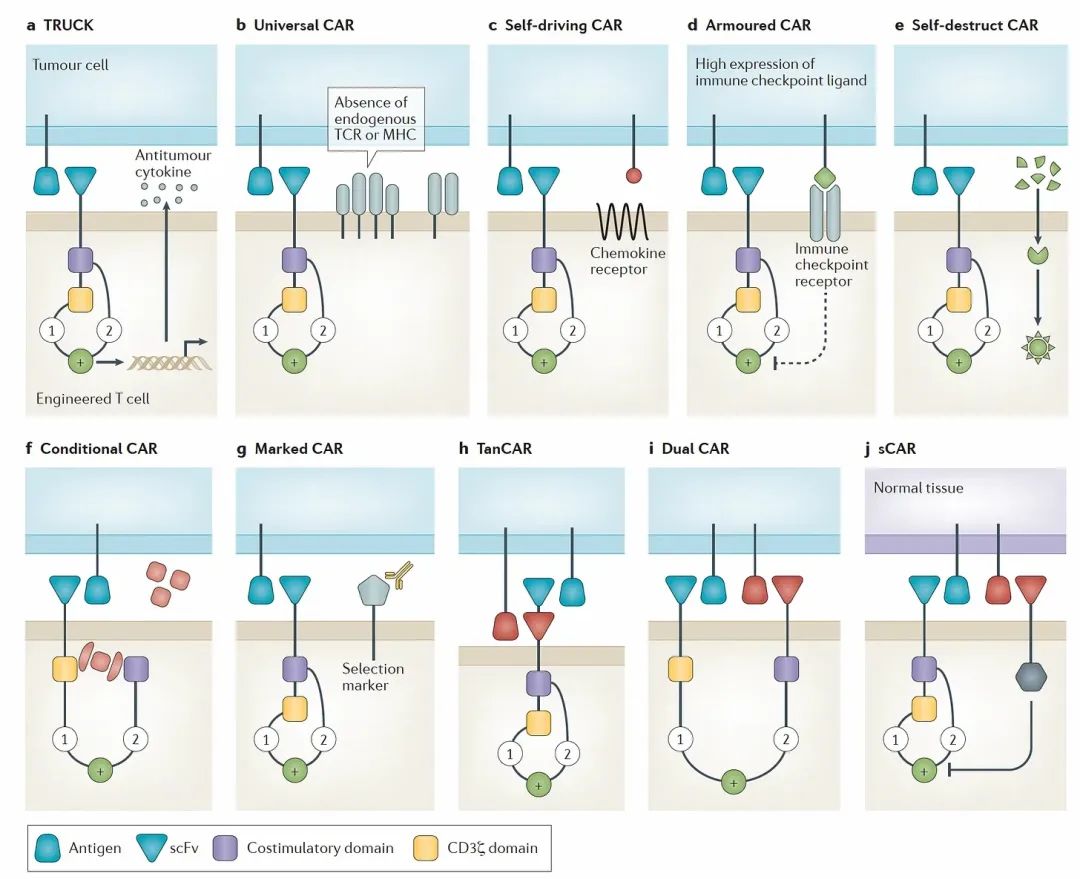
1. 對實體腫瘤的攻堅戰
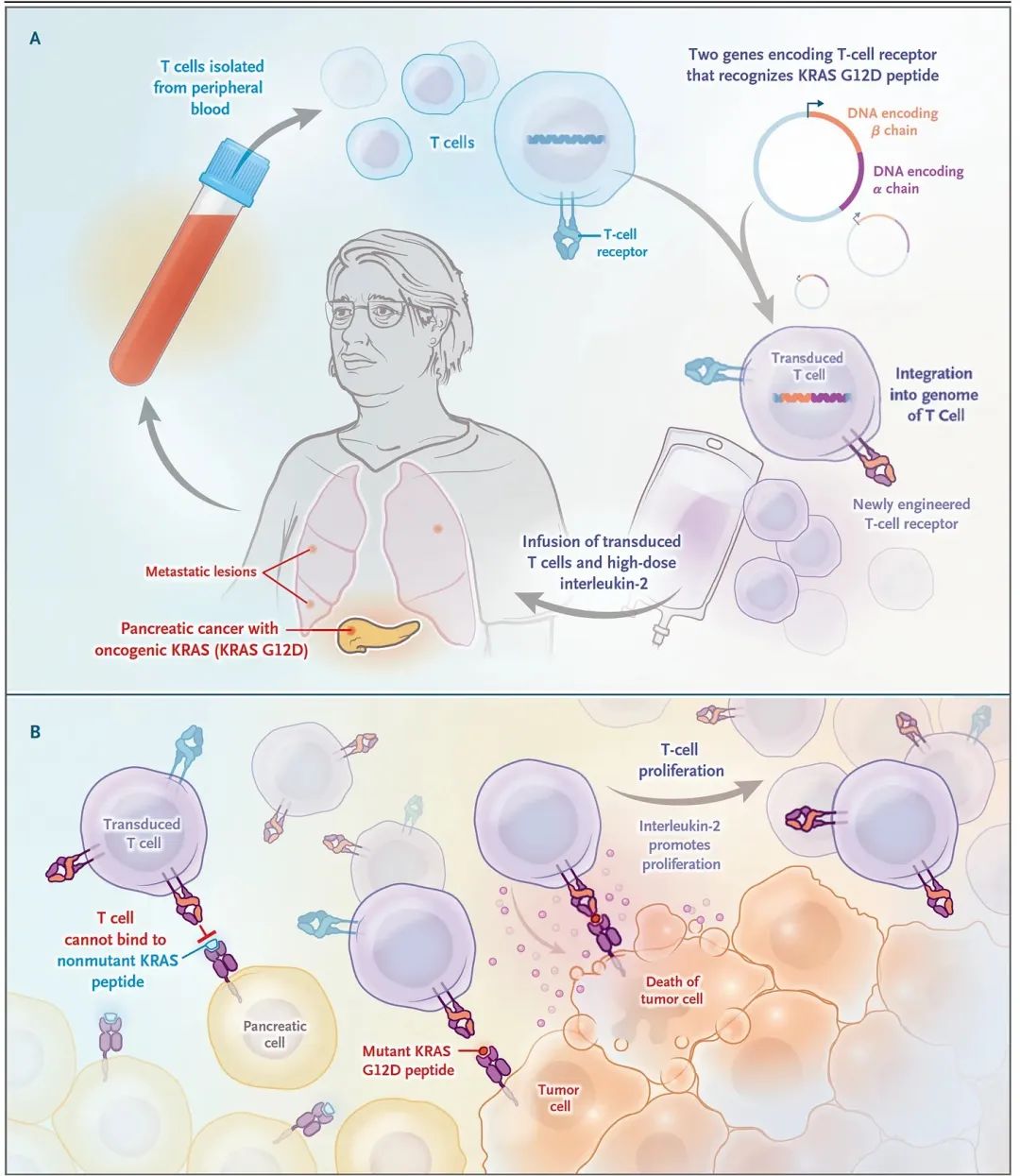
與此同時,在兒童中較為普遍的、致命性高度侵襲的腦癌和脊髓癌,即彌漫性內生性腦橋膠質瘤 (DIPG) 和彌漫性中線膠質瘤 (DMGs) 中,最近在4例患者中采用 CAR-T 療法,其中 3例表現出了明顯的改善。在這些案例中,靶向 GD2 的 CAR-T 被通過靜脈注射給患者,或直接原位注射到其腦腫瘤中。這項工作建立在 2017年一篇使用 CAR-T 靜脈注射治療膠質母細胞瘤患者的論文的基礎之上。
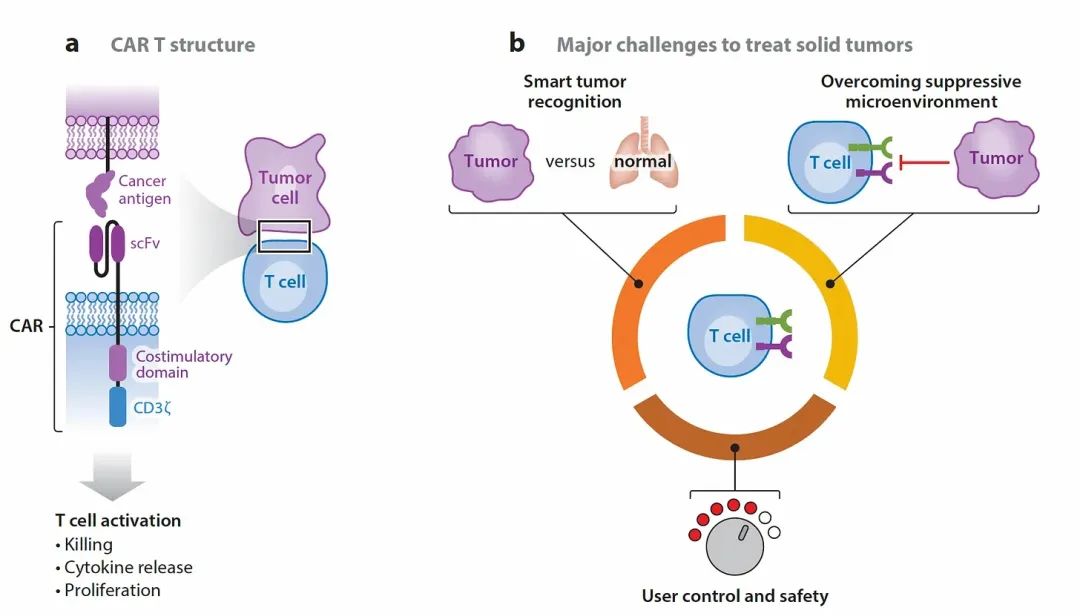
2. 自身免疫性疾病的初步試水
在癌癥治療中,構建 CAR-T 的目標是加強抗腫瘤免疫反應。與之相反,在自身免疫性疾病中,我們的目的正好相反。最近發表的 5例針對 CD-19 的 CAR-T 治療難治性紅斑狼瘡 (系統性紅斑狼瘡) 患者的例子表明,在沒有伴隨藥物治療的情況下,患者在大約 1年的隨訪期間取得了成功的緩解。值得注意的是其表現出的良好安全性。CAR-T 治療的主要問題是細胞因子釋放綜合征 (CRS) 和免疫效應細胞相關神經毒性綜合征 (ICANS),而這些副反應嚴重時可能會危及生命。除了系統性紅斑狼瘡,還有很多自身免疫性疾病可以成為 CAR-T 治療的目標領域。事實上,選擇性 CAR-T 干預,最近也已經開始被應用到多發性硬化癥的實驗模型中。這些進展為 CAR-T 的新應用鋪平了道路,其可被看作在未來選擇性地關閉靶向自身的不良免疫反應的開始。
3. 對抗纖維化(瘢痕)?:另辟蹊徑
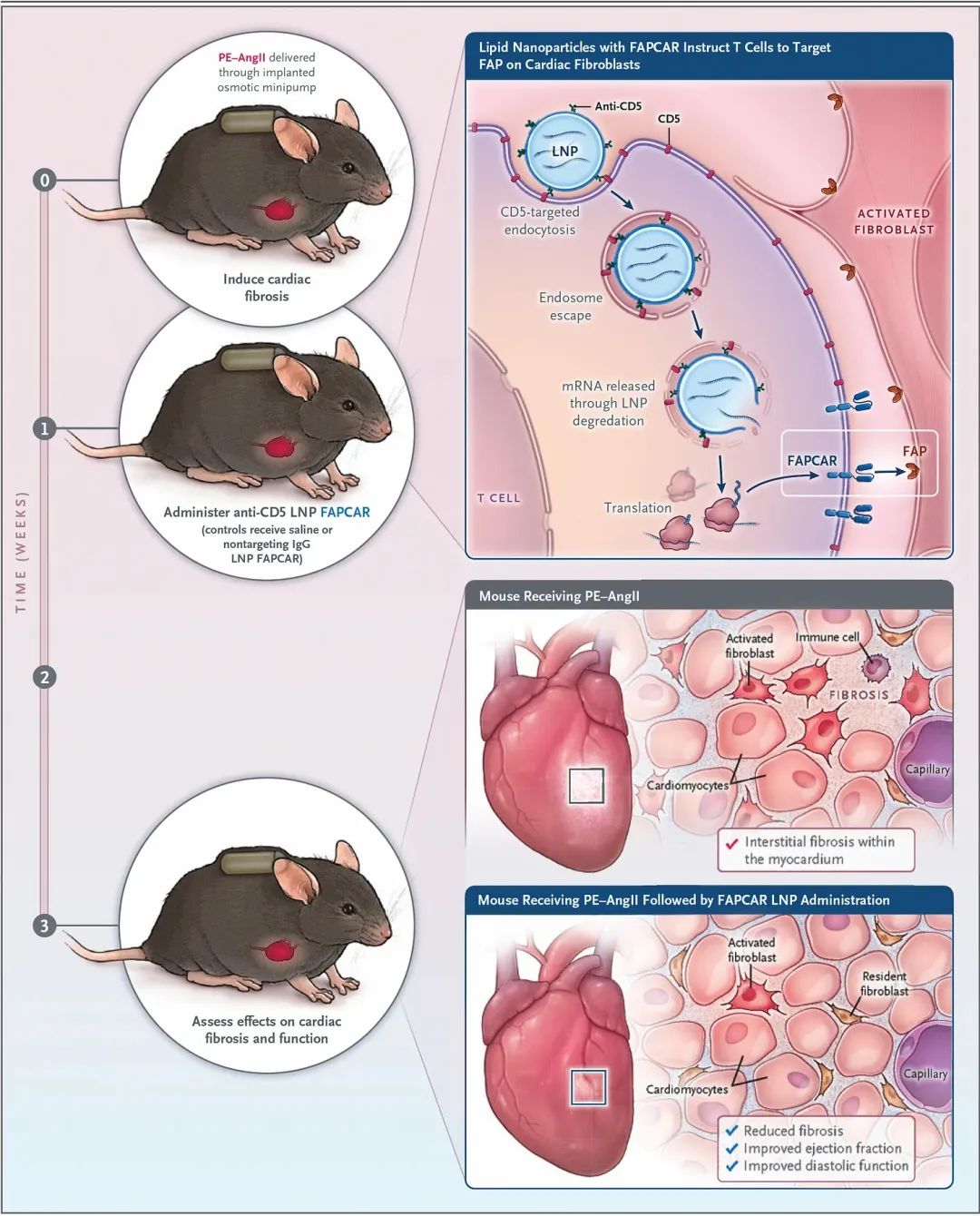
心臟的這種纖維化是許多致命疾病的根本原因,并且可以影響大多數器官,包括肝臟、腎臟、肺、骨髓和心臟。在高度工業化的國家中,這些疾病造成的死亡人數占死亡總數的 40%以上。同樣地,雖然這還是一項處于早期的研究工作,但它為細胞工程化方法解決長期未被滿足的需求奠定了基礎。在某些方面,這一成果更值得思考的也許是開創性地使用 CAR-T 靶向及逆轉衰老,而這種效果已經被研究者在一個實驗肺癌模型中觀察到。
4. T細胞工程的顯著增強
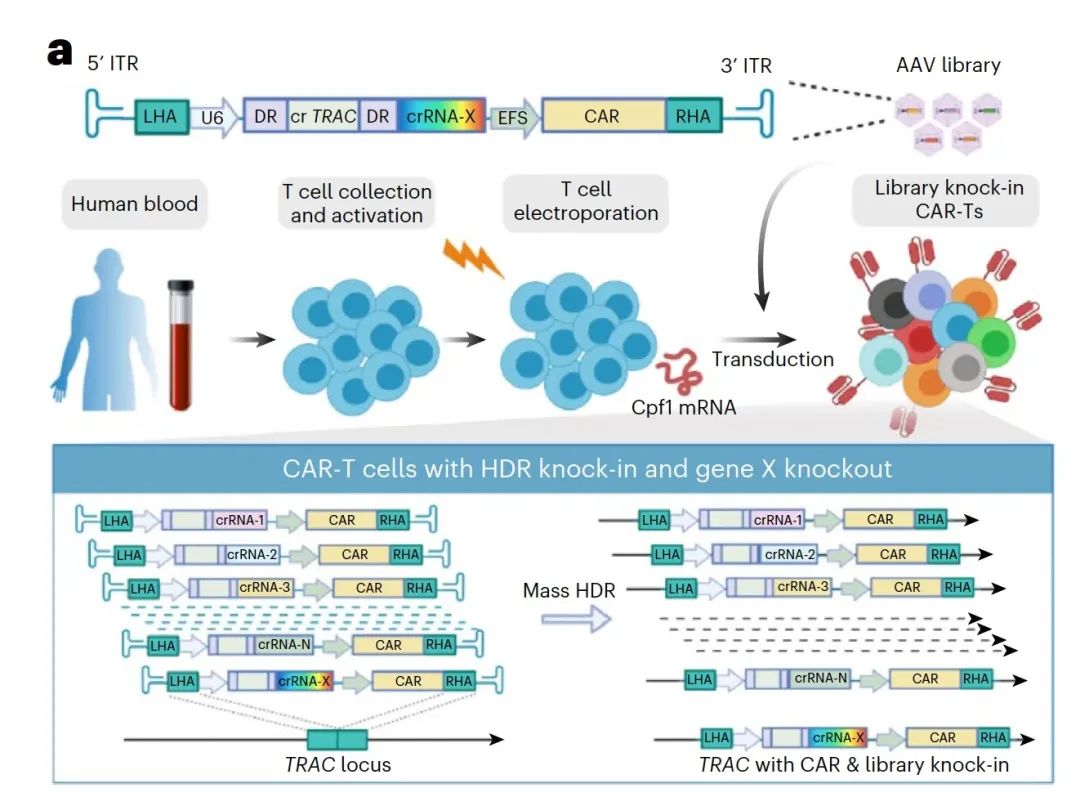
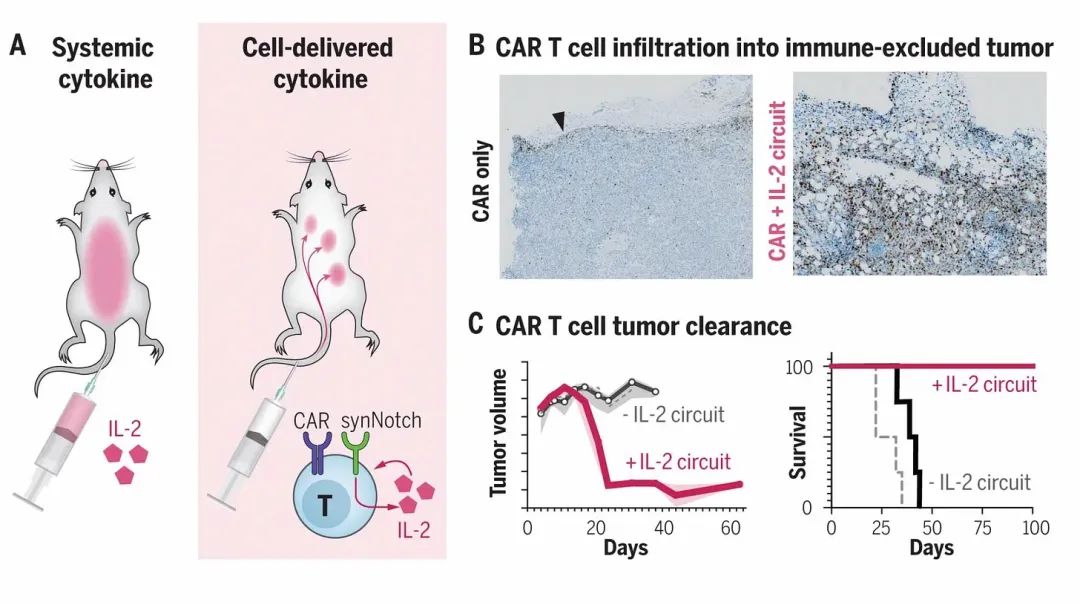
5. 現貨型 CAR-T (off-the-shelf CAR-T)
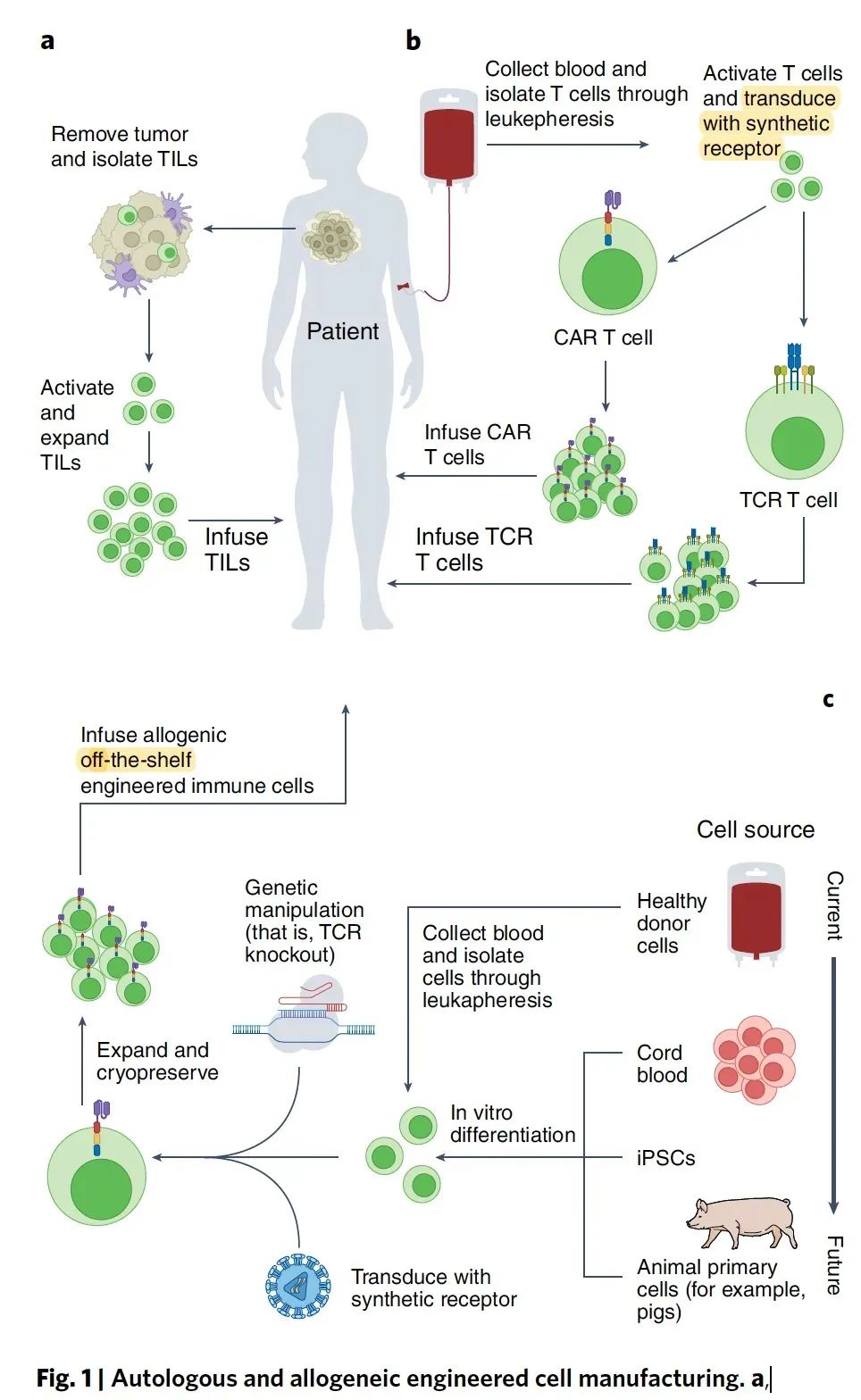
最后,我們再來談談 CAR-T 產業界多年來一直關注的現實落地問題。許多人認為,個體化的 CAR-T 產品幾乎永遠不可能成為主流療法,因為其單次治療的費用高達約 50萬美元(中國引進的國產化 CAR-T 也高達120萬人民幣),而這還不包括患者的住院費用和其他必要的輔助治療費用。要讓 CAR-T 惠及更多的潛在使用者,最重要的降低成本的方法也許就是使用現貨型 CAR-T (見本文頂部的示意圖)。最近,在 43名難治性多發性骨髓瘤患者中,現貨型 CAR-T 被證明是安全可行的方案,且實驗數據初步表明其展現出預期的療效。這種現貨型、流水化方案代表著大工業生產的趨勢,在未來或將取代費錢、費時、費力的定制化自體 CAR-T 路徑,后者是使用每個患者自己的 T 細胞進行定制化產生的。雖然現在還不能確定現貨型 CAR-T 是否能取得如自體 CAR-T 一樣好的療效和持久性,但毋庸置疑的是這些新發現將為解決這一主要障礙帶來了一些新的希望。
坦率地說,我們要對目前 CAR-T 領域所取得的飛速進展感到震驚,特別是最近幾周的進展。CAR-T 療法的潛在治療適應癥在不斷擴大,而細胞工程化技術的的增強讓其在治療我們尚無能為力的難治性疾病方面展現出了其獨特的優勢。隨著這種新興療法的潛力被不斷挖掘,自體 CAR-T 在不遠的將來或將如“舊時王謝堂前燕”那般,“飛入尋常百姓家”惠及千家萬戶。十年前,我們幾乎不會預料到這一領域會以如此蓬勃的勁頭快速發展。雖然仍存在許多嚴重的挑戰,比如可及性、醫療不平等等,但是我們有理由相信 CAR-T 及其相關技術正在變得離普羅大眾越來越近。
原文閱讀:https://erictopol.substack.com/p/engineering-t-cells
編輯:小果果,轉載請注明出處:http://www.448371.com/cells/myxb/24991.html
免責聲明:本站所轉載文章來源于其他平臺,主要目的在于分享行業相關知識,傳遞當前最新資訊。圖片、文章版權均屬于原作者所有,如有侵權,請及時告知,我們會在24小時內刪除相關信息。
說明:本站所發布的案例均摘錄于文獻,僅用于科普干細胞與再生醫學相關知識,不作為醫療建議。


 微信掃一掃
微信掃一掃  支付寶掃一掃
支付寶掃一掃