藥物開發的不同復雜程度
藥物開發的不同復雜程度
● ? ?● ? ? ●
生物醫藥的發展,從基礎研究到轉化研究,最終形成臨床治療產品,不是一蹴而就的。無論是最早的干細胞移植,還是現在的CAR-T治療,都是踩在巨人的肩膀上摸索慢慢實踐的。
?
從Thomas醫生開展最早的骨髓移植,并于1990年拿到諾貝爾獎開始,原創性的發現就不斷出現。從技術萌芽到形成最終產品,這需要歷經很長路程。比如,在1989年,第一代的CAR-T技術就嶄露頭角,但真正成功的應用到臨床,是在2012年賓夕法尼亞大學的Carl June實驗室和Stephan Grupp醫生一起治療白血病女孩Emily。一晃十年過去,Emily繼續保持完全緩解狀態,生活和健康人完全一樣。細胞治療為什么是繼小分子、大分子以后,可能的下一代治療技術或方式,主要是因為它能夠繼前面兩種治療方式之后,給目前無法治療的一些疾病患者帶來革命性的治療效果。
從產業層面來看,從2017年全球首個CAR-T產品上市,到現在已經有六款CAR-T的產品上市了。

圖1 ?細胞治療技術的發展歷程
一般來講,新興技術方面,監管都是落后于技術和產業發展的。比較成熟的發達國家,在現有細胞治療監管的政策下,也在監管方面做很多新的嘗試,設立專門的快速通道來支持細胞基因治療產品的發展。無論是美國FDA,還是歐盟EMA,基本上按照藥物管理模式來監管,并出臺了很多新的針對細胞基因治療產品的快速審評通道。
?
FDA出臺RMAT(Regenerative Medicine Advanced Therapy Designation),EMA出臺ATMP(先進醫學治療技術產品)。而我們的近鄰日本,為了在Yamanaka拿到諾貝爾獎以后能夠更快的發展細胞治療產業,選擇了雙軌制的發展思路。
?
總體而言,相對于小分子、大分子、化學藥等,細胞治療和基因治療還處于一個萌芽期,但是上升速度很快,目前也是跟國際比較接軌的賽道。



圖4 ?國際資本市場在細胞基因治療領域的投入情況

圖5 ?已批準的細胞治療藥物的價格

關于未來發展的趨勢。下圖7可以看到,根據ARM Reports數據,無論是科學界,還是工業界,有很多的細胞基因治療的產品正在做臨床試驗和臨床轉化。跟前些年相比,如果更多的項目或產品從早期研發階段開始進入到Phase II或者Phase III階段,那就離NDA和上市不遠了。
?
如果單純看適應癥的話,大部分集中在腫瘤領域。目前賽道非常擁擠,賽道里不單有細胞治療、基因治療,還有小分子和抗體。不過,細胞藥物現在開始往其他適應癥,比如自身免疫性疾病,神經退行性疾病,心腦血管疾病等方向去發展,其實對我們做創新來講,這可能是最便捷的一個方向,從市場空間來講,可能會比CAR-T晚期腫瘤更多,例如阿達木單抗,一個藥一年可能就能賣200億美金以上的銷售額,所以細胞療法用于自身免疫性疾病空間還是很大的,值得考慮。

–02–
中國細胞產業發展的歷史機遇
-
?上游:細胞存儲和設備試劑耗材
-
?中游:技術研發和新藥的轉化
-
下游:CDMO和臨床應用
▉??細胞治療產業鏈簡析
上游的細胞存儲是中國目前整個細胞產業鏈里面發展最成熟,市場競爭最激烈的領域,也是目前唯一可能會產生凈現金流的一個行業,而設備、耗材和試劑在未來可能是非常重要或潛在增長的領域。
?
中游無論是干細胞藥物研發還是以CAR-T為代表的免疫細胞藥物研發,已經有很多企業都在參與,而且有的企業已經上市了。近五年,細胞治療領域在國家政策的支持下發展是最快的。
?
下游的CDMO逐漸開始出現,規模也越做越大。未來在臨床上,隨著藥物獲批,技術轉化和成果的產生,如何能夠提高患者的治療效果以及遠期的生存質量,是臨床上需要去改進的地方。

圖8??中國藥品審評審批制度的改革
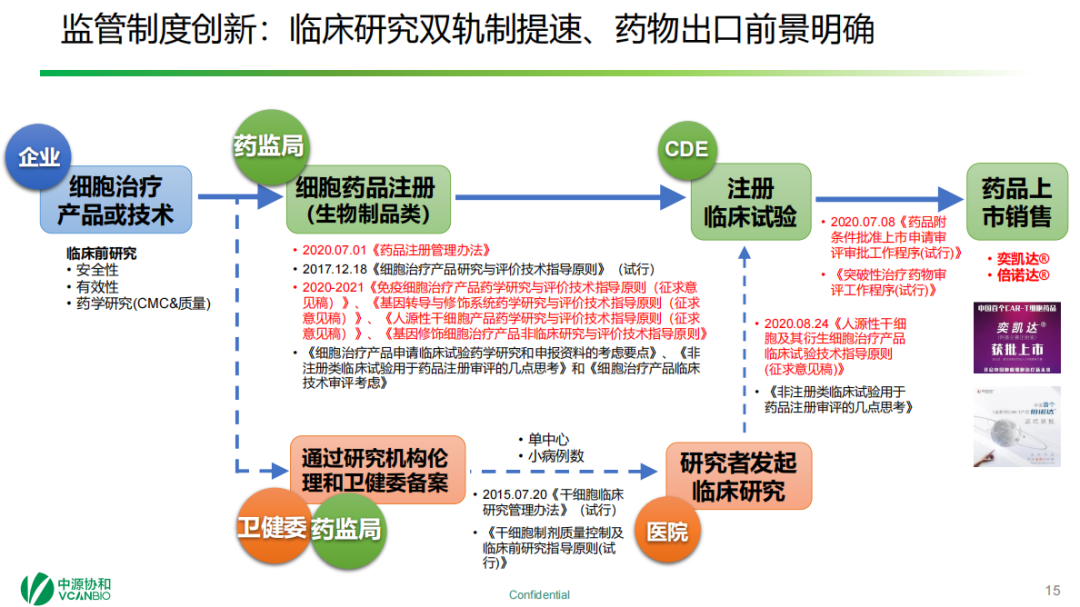
圖9? 細胞治療產品臨床研究的雙軌制


圖11? NMPA受理的CAR-T/TCR-T新藥

整個行業的發展除了技術和轉化外,也離不開資本市場的推動,這種現象在抗體藥物領域更為明顯。如今,新藥研發仍然是一個高投資、高風險的行業,特別是周期很長,如果僅靠一級市場的投資,特別是在此前主板市場對營利性有嚴格要求的情況下,其實很難獲得持續的投資。投完以后也要考慮資本的退出機制,以前是沒有通道的。近些年來,無論是港股18A的通道,還是科創板的第五類和最近北交所的通道,以及傳統納斯達克通道,允許未盈利的Biotech公司能夠IPO,并且能夠在二級市場持續的募資,以支持產品的繼續研究和轉化,這個資本退出通道的打開對于細胞治療產業能夠持續的發展是非常必要的。
?
到目前為止,國內的細胞治療產業有五家公司已經成功上市,整體市值超400多億人民幣。

▉??挑戰一:上游的細胞存儲和設備耗材市場
-
新生兒人口的快速下降,導致細胞存儲的市場開始慢慢的變小;
-
已上市產品大部分用的設備試劑耗材都是國外進口,價格昂貴;
▉??挑戰二:二級市場表現不佳,一二級市場倒掛,“資本寒冬”到來
-
二級市場上Cell治療、IO、Gene Therapy和RMAT上市公司表現不佳;
-
2022年4月以來中國藥企募資明顯降低,環比減少45%,同比減少63%;
-
到2022年4月,港股生物科技指數連續10個月下跌,距最高點已下跌近62%;
▉??挑戰三:靶點扎堆同質化發展與知識產權保護
-
細胞治療領域的靶點扎堆與同質化發展問題。無論是國際還是國內,大家集中的靶點非常一致,例如EGFR,PD1,PDL1,CD19,JAK等; -
知識產權保護目前階段在我國可能還沒有深入研究或重視。我國雖然專利申請的數量比較多,現在也有一些授權,但真正能夠完完全全保護住自己專利的有多少,是值得深入研究的。出海時面臨的專利訴訟風險非常大,這在美國已經發生過;
-
發展高科技產品與技術面臨著不同領域的競爭,這就要求領域內的領先企業必須要關注,不僅是中國,而且是國際上的最前沿技術;
-
在臨床階段,已上市的一些產品開始慢慢從末線病人向二線甚至一線發展,但該發展不是隨便就能推動,充滿了挑戰;
-
此外,產品由末線向前線的發展,對資金的投入、團隊的運營以及整個過程的監管具有很大挑戰;
-
無論是在干細胞領域還是CAR-T領域,整個中國目前比較缺乏有細胞治療臨床研究經驗的醫生;
-
新藥研究是一個高風險、高投入、高回報、長周期的過程,每一步都需要按照現有的相關法規和實驗去嚴格驗證,這對細胞治療產品同樣如此,不同的階段需要專業的研究團隊來驗證,只有這樣才能將產品從最早的Discovery階段推向上市,中間的CMC過程是一個持續改進的過程,該過程充滿了挑戰。 -
商業化階段要以終為始,做產品前一定要判斷是什么是真正的未被滿足的臨床需求,而不能盲目的去研發。同時細胞治療產品與患者打交道次數多,目前價格昂貴,因此更多的是提供服務,而不僅僅單純是銷售產品,所以整個流程需要更用心的經營。
-
目前的類雙軌制比較適合我們的國情,未來如果想要進一步提高細胞治療產品IND和轉化的速度,可以參考成熟國家的快速通道,例如FDA的RMAT和歐盟藥監局的ATMP,希望我們國家監管部門有專門針對這類產品的通道來加速產品在注冊以及臨床轉化的過程。
總結而言,細胞治療產業的發展需要打造一個生態系統,因為細胞治療產業的技術是走在前面的,特別需要政產學研醫再加上資本和媒體一起來推動,在這個過程中有很多的環節需要不同領域的人才積極加入進來,一起推動它的轉化。
–04–
▉??全球細胞治療產業發展現狀
▉??中國細胞治療產業發展的歷史機遇
▉??未來細胞治療產業鏈發展挑戰
?張宇博士??
?
編輯:小果果,轉載請注明出處:http://www.448371.com/zixun/hydt/14511.html
免責聲明:本站所轉載文章來源于其他平臺,主要目的在于分享行業相關知識,傳遞當前最新資訊。圖片、文章版權均屬于原作者所有,如有侵權,請及時告知,我們會在24小時內刪除相關信息。
說明:本站所發布的案例均摘錄于文獻,僅用于科普干細胞與再生醫學相關知識,不作為醫療建議。



 微信掃一掃
微信掃一掃  支付寶掃一掃
支付寶掃一掃