2023年開端, CAR-T細胞療法可謂是喜憂參半。在國內,人民日報健康客戶端梳理了10款有望獲批的藥物,其中有3款CAR-T,分別靶向BCMA(治療多發性骨髓瘤)和CD19(治療白血病)。在國外,《柳葉刀》報道了CD19 CAR-T成功治療患有自身免疫疾病-抗合成酶抗體綜合征(ASS)的患者。但是市場方面,全球首款CAR-T療法銷售額下跌9%。
CAR-T療法利用免疫細胞殺傷作用的特異性、持久性,為腫瘤患者提供更精準、長效的治療模式,在多種造血惡性腫瘤中具有顯著的抗腫瘤活性。全球已有多款靶向CD19和BCMA的細胞產品上市。
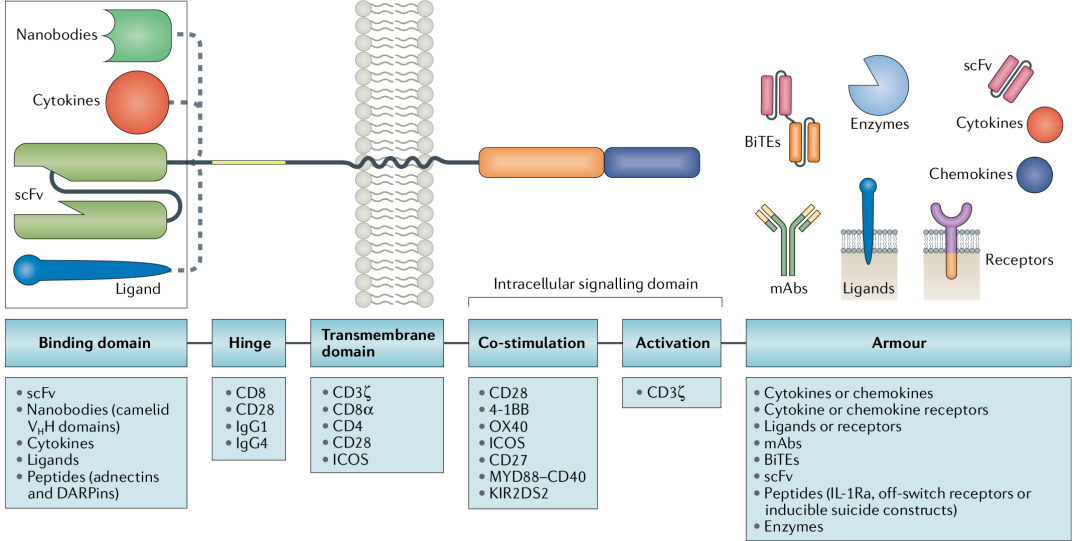
CAR(嵌合抗原受體)由靶向結合抗原的單鏈抗體可變區、鉸鏈跨膜區和胞內信號傳導結構域構成的重組跨膜分子,CAR基因可通過多種病毒或非病毒載體在體外轉導至T細胞,所制備的CAR-T細胞在回輸后可遷移、重定向至腫瘤細胞并廣泛增殖發揮細胞毒性作用。從美國臨床試驗官網查詢到用于淋巴瘤的CAR-T最多,其它依次是為急性淋巴細胞性白血病(ALL)、多發性骨髓瘤(MM)、慢性淋巴細胞性白血病(CLL)、急性髓細胞性白血病(AML)。
CAR-T療法的一些瓶頸限制其廣泛應用,如毒副作用嚴重、抗原逃逸、治療持續性、異質性等,特別是在實體瘤中治療效果有限。主要有:
第一,CAR-T細胞衰竭。比如有的患者自身T細胞無法成功生產CAR-T細胞,或者生成的CAR-T細胞擴增不充分。有些患者有限的持久性是疾病復發的潛在因素。
第二,抗原調節。如惡性B細胞上CD19或CD22的丟失或下調,造成抗原逃逸,對CAR-T療法產生抗藥性。
第三,CAR-T療法毒性,主要是嚴重的細胞因子釋放綜合征(CRS)和神經毒性。關于CRS的治療是否干預CAR緩解的持久性影響還在研究中。
第四,未知的疾病機制,這是正在進行的研究工作的重點,以優化CAR-T細胞療法的臨床應用。
CAR主要組成部分:抗原結合域、鉸鏈、跨膜域和細胞內信號域。每部分有不同的功能,組成部件的多樣化組合,可以實現CAR分子的優化設計。抗原結合域常為單鏈抗體(scFv),負責識別并結合靶抗原。鉸鏈和跨膜域可將scFv錨定于細胞膜上。胞內信號域由共刺激因子和CD3信號域組成。當抗原被識別和結合后,產生刺激信號傳至胞內信號域,T細胞被激活并發揮效應功能。
對于CAR-T治療過程中出現的細胞因子風暴和神經毒性,主要是干預細胞因子的分泌或控制T細胞的過度激活,如通過抗體阻斷IL-1、IL-6和GM-CSF,進而阻斷過度的炎癥反應。面對治療過程中產生抗性的問題,可以通過設計多靶向的CAR分子或增加靶抗原的表達來改善,或是提高scFv與靶抗原的親和力,也可能有助于CAR-T細胞識別低密度的靶抗原。
目前CAR-T的制造多使用患者的異質性T細胞。某些特定T細胞亞群修飾的CAR-T細胞可能會產生更好的效果。制造通用型細胞是未來發展的方向。有一種形式是抗體帶上生物素等標簽,與抗原結合后標記腫瘤細胞,然后針對這個標簽開發的 CAR-T 細胞就會被激活,發揮細胞殺傷功能。
CAR-T細胞研究試驗圍繞療效、毒性和耐藥性展開,以尋找新型靶點、闡明信號機制為基礎,結合新型技術的應用,通過CAR設計、轉導方法和最佳細胞類型的不斷研究,必將提高CAR-T治療效果,并適用于更多類型癌癥患者的治療。
義翹神州CAR-T開發綜合解決方案
作為一家專注于為全球生物醫藥領域提供關鍵試劑和技術服務的高新技術企業,義翹神州特地推出了綜合性的CAR-T細胞療法開發解決方案,全方位地支持客戶更方便、更快速地完成從早期靶點發現到臨床前研究的每一個階段。
1. Xiaoyu Wang, et al. Recent advances in lentiviral vectors for gene therapy.
2. Natalia Elizalde and Juan Carlos Ramírez. Lentiviral vectors: key challenges and new developments.
3. Michael C. Milone and? Una O’Doherty. Clinical use of lentiviral vectors.
4. David Escors, Karine Breckpot. Lentiviral vectors in gene therapy: their current status and future potential.
5. Merten OW, Hebben M, Bovolenta C. Production of Sakuma,T.,Barry, M. A. and Ikeda, Y. Lentiviral vectors : basic to translational.
6. Fabian, et al. CD19-targeted CAR-T cells in refractory antisynthetase syndrome.
編輯:小果果,轉載請注明出處:http://www.448371.com/cells/myxb/25984.html
免責聲明:本站所轉載文章來源于其他平臺,主要目的在于分享行業相關知識,傳遞當前最新資訊。圖片、文章版權均屬于原作者所有,如有侵權,請及時告知,我們會在24小時內刪除相關信息。
說明:本站所發布的案例均摘錄于文獻,僅用于科普干細胞與再生醫學相關知識,不作為醫療建議。




 微信掃一掃
微信掃一掃  支付寶掃一掃
支付寶掃一掃