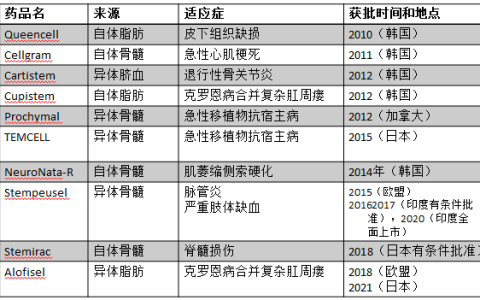
“ 肌肉萎縮癥是一類因不同病因而導(dǎo)致肌肉力量減退的疾病,其中Ullrich型先天性肌肉萎縮癥(UCMD)作為COL6相關(guān)肌病的末端終結(jié),不光會(huì)剝奪患者的行動(dòng)力與智力,嚴(yán)重時(shí)還會(huì)危及患者生命。 幸運(yùn)地是,這個(gè)“不治之癥”正在被攻克,日本京都大學(xué)iPS細(xì)胞研究與應(yīng)用中心(CiRA)發(fā)現(xiàn):利用基于iPSC技術(shù)衍生的間充質(zhì)干細(xì)胞(MSCs)能恢復(fù)先天性肌肉萎縮癥小鼠的肌肉再生,為疾病的治療帶來(lái)了新的方案。

皮膚下的肌肉可能是最為神奇的人體引擎。
它支持著我們走路、跑跳,甚至攀登上陡峭的山峰。也正是這600余塊肌肉的緊密合作,我們的日常行動(dòng)才得以為繼。
然而有這么一群人,從出生就被剝奪了行動(dòng)的權(quán)利,他們患上了一種叫“Ullrich型先天性肌肉萎縮癥(UCMD)”的罕見(jiàn)病,是由人體編碼膠原蛋白Ⅵ(包括COL6A1,COL6A2和COL6A3)發(fā)生基因突變所導(dǎo)致的。
患兒從小就會(huì)出現(xiàn)肌無(wú)力,無(wú)法獨(dú)立行走等問(wèn)題,待到年齡漸長(zhǎng),他們還得依靠呼吸機(jī)維持夜間呼吸,否則極易因呼吸衰竭而死亡。
更令人絕望的是,作為最嚴(yán)重的COL6相關(guān)肌病,醫(yī)學(xué)界對(duì)此也束手無(wú)策,難道只有眼睜睜地看著疾病愈演愈烈嗎?
11月23日,國(guó)際期刊《Frontiers in Cell and Developmental Biology》(影響因子:6.684)給出了新答案。

△ 研究發(fā)現(xiàn):干細(xì)胞促進(jìn)患有罕見(jiàn)肌肉疾病的小鼠肌肉恢復(fù)再生
來(lái)自日本京都大學(xué)iPS細(xì)胞研究與應(yīng)用中心(CiRA)的研究者[1]發(fā)現(xiàn):通過(guò)iPSC衍生的間充質(zhì)干細(xì)胞(iMSC),可以系統(tǒng)性地恢復(fù)膠原蛋白VI合成,幫助UCMD小鼠肌肉再生。這一結(jié)果為有UCMD患兒的家庭點(diǎn)燃了希望。
8周握力提高35%? iPSC帶來(lái)治療新策略
近年炙手可熱的iPSC細(xì)胞技術(shù)相信大家都有所耳聞。
這項(xiàng)被譽(yù)為“改變世界的偉大技術(shù)”,意味著研究人員可以用機(jī)體的多種不同來(lái)源的細(xì)胞進(jìn)行重新編碼,將它們轉(zhuǎn)化為具有萬(wàn)能分化性的誘導(dǎo)多能干細(xì)胞(iPSC),進(jìn)而分化成干細(xì)胞、神經(jīng)細(xì)胞、或者是其他需要再生的細(xì)胞。

△iPSC技術(shù)正在改變世界。它能量產(chǎn)血小板(左圖上),支持3D打印心臟(右圖上)再生毛囊干細(xì)胞(左圖下),定向分化成T細(xì)胞(右圖下)
此項(xiàng)UCMD實(shí)驗(yàn)中選用的便是iPSC技術(shù)衍生的間充質(zhì)干細(xì)胞(iMSC)。
可能有人會(huì)疑問(wèn):為何不直接提取自身骨骼肌中的MSCs,反而要經(jīng)iPSC技術(shù)“曲線救國(guó)”呢?
對(duì)此,該研究的Aya Harada博士是這樣考慮的:“雖然源自其他組織的MSCs理論上也能產(chǎn)生膠原VI,但運(yùn)用iPSC可以制備大量具有均勻質(zhì)量的細(xì)胞用于移植。”簡(jiǎn)而言之,iPSC衍生細(xì)胞在“量產(chǎn)”上更具優(yōu)勢(shì)。
而在動(dòng)物模型選擇上,基于前人經(jīng)驗(yàn),研究者選擇了在敲除Col6a1基因、獲得NSG (NOD酸γ)背景后雜交獲得的Col6a1KO/NSG小鼠。這些小鼠都被安排了腹腔注射5×10?iMSCs。部分小鼠還在第4周進(jìn)行了i.p.加強(qiáng)移植(23G 1ml注射器注射5 × 10?個(gè)iMSCs )。
待到第8周進(jìn)行數(shù)據(jù)統(tǒng)計(jì)時(shí),研究者重點(diǎn)觀測(cè)了這些被安排i.p.移植小鼠,追蹤指標(biāo)為膠原蛋白VI的挽救面積、肌肉的再生情況,同時(shí)也對(duì)線粒體形態(tài)和細(xì)胞凋亡情況,肌肉功能進(jìn)行了檢測(cè),結(jié)果發(fā)現(xiàn):
?
1、與未移植的小鼠相比,移植iMSC的小鼠在第8周肌肉重量明顯增加;
2、在移植小鼠中,多核的肌纖維的數(shù)量增加且多核肌纖維與單核肌纖維的比例提高;
3、iMSC移植減少了畸形線粒體和肌肉細(xì)胞的凋亡數(shù)量。
4、8周后,iMSC移植的小鼠握力較之未移植小鼠提高了35%,旋轉(zhuǎn)能力也提升近30%。
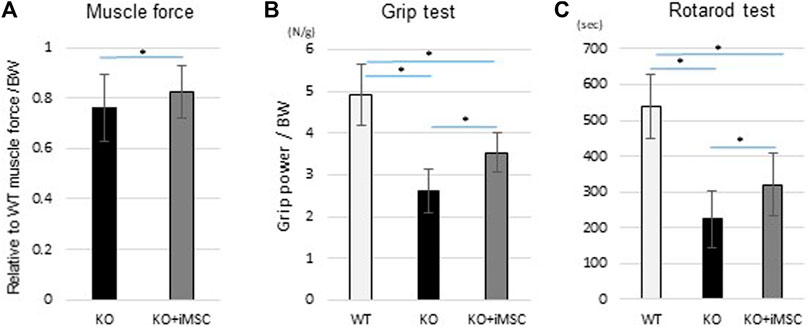
△iMSC移植小鼠在8周時(shí)旋轉(zhuǎn)及握力功能均得到改善
但實(shí)驗(yàn)并未到此為止,為了確認(rèn)iPSC衍生iMSC的安全性,在接下來(lái)的20周研究者依舊保持著觀察,而直至實(shí)驗(yàn)結(jié)束,小鼠并未出現(xiàn)不良反應(yīng)或致瘤事件。
綜上所述,iPSC技術(shù)具有治療UCMD的潛力。
全能分化性+抑制凋亡? iPSC起效關(guān)鍵
在這項(xiàng)研究中,iPSC技術(shù)之所以能夠起效,關(guān)鍵還在于iPSC的全能分化性與抑制細(xì)胞凋亡的特性。
UCMD發(fā)病機(jī)制是由于編碼膠原蛋白Ⅵ(COL6A1-3)上的基因發(fā)生突變,繼而對(duì)膠原蛋白VI的合成、組裝、分泌等產(chǎn)生影響。也就是說(shuō),在UCMD中,膠原蛋白VI是關(guān)鍵物質(zhì)。
得益于iPSC細(xì)胞的全能分化特性,這群經(jīng)iPSC衍生的iMSC幾乎保持了和骨骼肌原始MSC相似的基因及蛋白表達(dá)水平,同樣能發(fā)揮修復(fù)再生體內(nèi)組織的功能。我們?cè)陔S后的實(shí)驗(yàn)中也能看到,iMSC展現(xiàn)了長(zhǎng)時(shí)間分泌膠原VI的能力,以增強(qiáng)膠原VI恢復(fù)部位的肌肉再生。
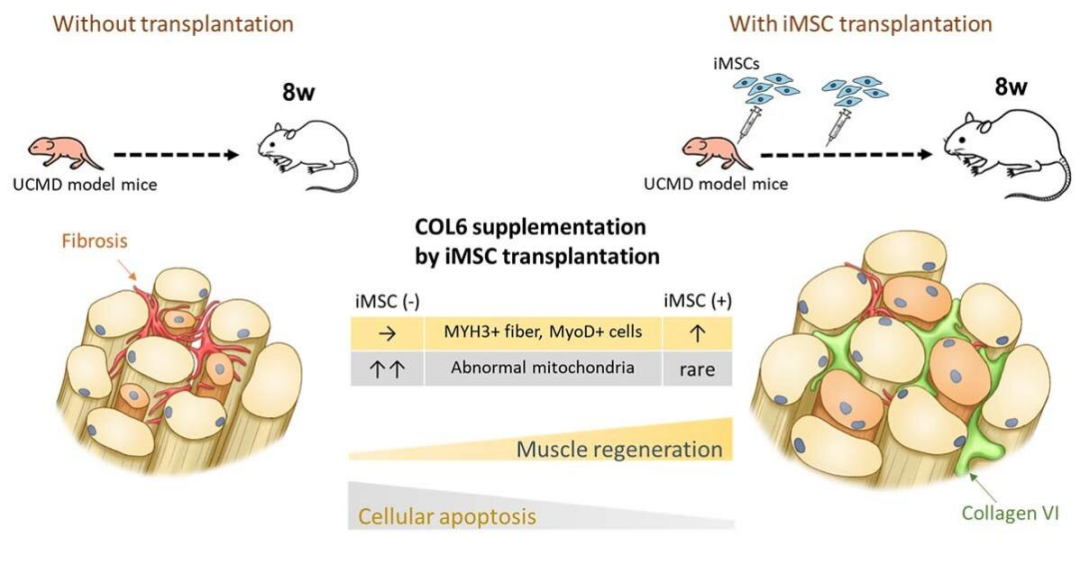
△Hidetoshi Sakurai實(shí)驗(yàn)室展示了iPS細(xì)胞如何補(bǔ)充膠原VI以再生患有Ullrich先天性肌肉萎縮癥的小鼠的肌肉。圖片來(lái)源:京都大學(xué)
而在實(shí)驗(yàn)中,UCMD小鼠的線粒體還呈現(xiàn)出異常狀態(tài),也由此加速了肌肉細(xì)胞的凋亡,這種情況在移植iMSC后得到了改善,這里就要說(shuō)到干細(xì)胞的旁分泌特性了。

△未移植Col6KO/NSG小鼠8周四頭肌的電子顯微照片(A)箭頭處為線粒體異常,移植iMSC小鼠線粒體(B)異常極少
大量實(shí)驗(yàn)證實(shí):干細(xì)胞可以分泌各類生長(zhǎng)因子、細(xì)胞因子,如血管內(nèi)皮生長(zhǎng)因子(VEGF),肝細(xì)胞生長(zhǎng)因子(HGF),胰島素樣生長(zhǎng)因子等,這些因子都能參與調(diào)節(jié)細(xì)胞微環(huán)境,防止肌肉細(xì)胞提前凋亡。
?
不止于UCMD
干細(xì)胞帶來(lái)更多希望
前文我們就提到過(guò),肌肉萎縮其實(shí)是一系列不同病因而導(dǎo)致肌肉力量減退的疾病,所涉病種十分廣泛,除了上述提到的UCMD,還有進(jìn)行性肌肉萎縮癥,脊髓性肌萎縮等,而干細(xì)胞在它們的應(yīng)用治療上也均有建樹(shù)。
脊髓型肌萎縮是一種由脊髓前角運(yùn)動(dòng)神經(jīng)元變性導(dǎo)致的肌無(wú)力、肌萎縮的疾病,主要是由SMN1基因突變導(dǎo)致,患者主要表現(xiàn)為進(jìn)行性、對(duì)稱性四肢和軀干肌無(wú)力,萎縮,重癥患兒常死于呼吸衰竭。
那干細(xì)胞療法可以治療嗎?2012年《Science Translational Medicine》(影響因子:17.956)發(fā)表一項(xiàng)研究[2],意大利的科學(xué)家們從SMA患者的皮膚成纖維細(xì)胞產(chǎn)生并經(jīng)遺傳矯正的iPSC細(xì)胞用于自體細(xì)胞療法,他們?cè)谛∈竽P椭谐晒刂谱×思膊〉倪M(jìn)展。

△經(jīng)基因校正的 SMA-iPSCs 在分化為運(yùn)動(dòng)神經(jīng)元后可能為 SMA 的治療性移植提供運(yùn)動(dòng)神經(jīng)元的來(lái)源
研究者之一的米蘭大學(xué)Stefania Corti表示:“理想的脊髓性肌萎縮治療方法將是一種組合治療策略,用分子治療解決遺傳缺陷,用細(xì)胞移植補(bǔ)充性地應(yīng)對(duì)疾病病癥。”
進(jìn)行性肌肉萎縮癥
這個(gè)疾病案例發(fā)生在中國(guó),CCTV-1《人口》欄目曾報(bào)道過(guò)一對(duì)患有”進(jìn)行性肌肉萎縮癥”的雙胞胎兄弟[3]。這種肌肉萎縮也是由于基因缺陷導(dǎo)致的,基本無(wú)藥可醫(yī)。
還好母親蔡麗萍并沒(méi)有放棄希望,她偶然在電視中看到有醫(yī)院正通過(guò)干細(xì)胞移植治療疾病,就與院方取得了聯(lián)系。
在經(jīng)過(guò)從孩子體內(nèi)抽取一定數(shù)量的骨髓干細(xì)胞,進(jìn)行細(xì)胞分離,培養(yǎng)和誘導(dǎo)分化后,這些被寄予厚望的干細(xì)胞被移植回孩子體內(nèi)。
結(jié)果手術(shù)非常順利,在20天之后,雙胞胎中的彬彬就可以靠墻站住,而在接下來(lái)的2年間,經(jīng)過(guò)4次干細(xì)胞移植手術(shù),兩個(gè)孩子已經(jīng)能走路。

△兄弟兩正在接受康復(fù)訓(xùn)練,這將是一個(gè)漫長(zhǎng)而充滿希望的過(guò)程
干細(xì)胞這項(xiàng)新技術(shù)的應(yīng)用讓他們的癥狀得到緩解與好轉(zhuǎn),改善了患者的生活質(zhì)量。
隨著全球范圍內(nèi)相關(guān)研究的不斷深入,干細(xì)胞已經(jīng)在多種會(huì)導(dǎo)致肌肉萎縮癥的疾病臨床中展現(xiàn)了其威力,隨著這些“不治之癥”被逐漸攻克,讓罹患肌肉萎縮癥的病患重新站起來(lái),過(guò)上正常人的生活,將不再是夢(mèng)想。
Write in the last
寫在最后
不止于UCMD,不止于肌肉萎縮相關(guān)疾病,干細(xì)胞療法正以不可抵擋的勢(shì)頭挑戰(zhàn)著多種疑難雜癥,雖然再生醫(yī)學(xué)之路無(wú)法一日千里,但隨著探索的車輪不斷向前,我們翹首以盼的明天,終將逐一實(shí)現(xiàn)。
部分圖片來(lái)自網(wǎng)絡(luò)
參考資料:
[1]?Systemic Supplementation of Collagen VI by Neonatal Transplantation of iPSC-Derived MSCs Improves Histological Phenotype and Function of Col6-Deficient Model Mice.?https://doi.org/10.3389/fcell.2021.790341
[2]?Genetic correction of human induced pluripotent stem cells from patients with spinal muscular atrophy. https://doi.org/10.1126/scitranslmed.3004108
[3] CCTV-1《人口》欄目:站起來(lái)的“面條”兄弟
編輯:小果果,轉(zhuǎn)載請(qǐng)注明出處:http://www.448371.com/cells/gxb/7973.html
免責(zé)聲明:本站所轉(zhuǎn)載文章來(lái)源于其他平臺(tái),主要目的在于分享行業(yè)相關(guān)知識(shí),傳遞當(dāng)前最新資訊。圖片、文章版權(quán)均屬于原作者所有,如有侵權(quán),請(qǐng)及時(shí)告知,我們會(huì)在24小時(shí)內(nèi)刪除相關(guān)信息。
說(shuō)明:本站所發(fā)布的案例均摘錄于文獻(xiàn),僅用于科普干細(xì)胞與再生醫(yī)學(xué)相關(guān)知識(shí),不作為醫(yī)療建議。


 微信掃一掃
微信掃一掃  支付寶掃一掃
支付寶掃一掃