作為腫瘤治療的新方法,生物治療目前被認(rèn)為是最有希望攻克癌癥的方法之一。2013年科學(xué)界頂級(jí)雜志《Science》把腫瘤的免疫治療列為2013年的十大科學(xué)突破之首,與腫瘤免疫治療有關(guān)的基礎(chǔ)研究和臨床應(yīng)用在世界各地全面開展,并取得一系列重大突破,CAR-T細(xì)胞治療技術(shù)就是其中的典型代表。
在所謂的“液體癌癥”,如白血病和淋巴瘤的治療中取得了重大成功。多家企業(yè)CAR-T產(chǎn)品在血液流瘤賽道爭(zhēng)奪,使得該市場(chǎng)空間相對(duì)較小,而細(xì)胞治療的實(shí)體腫瘤市場(chǎng)空間巨大,有觀點(diǎn)指出,從血液瘤延伸至實(shí)體瘤會(huì)是CAR-T研究的一個(gè)大趨勢(shì)。
CAR-T治療實(shí)體腫瘤面臨的挑戰(zhàn)
實(shí)體腫瘤和血液腫瘤本身特質(zhì)存在著很大的差異,治療實(shí)體腫瘤存在很多問題。實(shí)體腫瘤一個(gè)突出的特點(diǎn)是異質(zhì)性。對(duì)于同一個(gè)患者,在一個(gè)部位的腫瘤也不一定表達(dá)相同的腫瘤相關(guān)性抗原,即使在同一個(gè)腫瘤病灶上,也沒有一種抗原可以覆蓋全部的腫瘤細(xì)胞。高度異質(zhì)性使實(shí)體腫瘤的治療難度大大增加,靶點(diǎn)的選擇也成為了CAR-T治療實(shí)體腫瘤面臨的重大挑戰(zhàn)。
另外,CAR-T細(xì)胞的體內(nèi)歸巢與活化維持也是個(gè)棘手的問題。如何將輸注的CAR-T細(xì)胞從外周血中精準(zhǔn)地歸巢至腫瘤部位并發(fā)揮殺傷作用,仍然是一個(gè)巨大的挑戰(zhàn),通過基因工程手段來修飾CAR-T細(xì)胞以增強(qiáng)其抗瘤活性也成為了當(dāng)前的研究熱點(diǎn)。
國(guó)外實(shí)體瘤研究進(jìn)展

La Jolla免疫學(xué)研究所(LJI)研究人員Anjana Rao教授過去幾年中一直致力于解開這其中的原因,其研究組發(fā)表了一系列論文,發(fā)現(xiàn)了一種調(diào)節(jié)基因表達(dá)的轉(zhuǎn)錄因子:NFAT能打開“下游”基因,削弱T細(xì)胞對(duì)腫瘤的反應(yīng),使T細(xì)胞衰竭。Anjana Rao教授作為美國(guó)科學(xué)院院士,在免疫研究領(lǐng)域功成名就,并且在表觀遺傳領(lǐng)域也取得了許多傲人的成績(jī)。
近期其團(tuán)隊(duì)又報(bào)道了一組這些下游基因編碼的轉(zhuǎn)錄因子——NR4A,腫瘤浸潤(rùn)的CAR-T細(xì)胞中NR4A蛋白被剔除,能改善腫瘤排斥。然而,在該途徑中與NFAT和NR4A合作的其他參與者的身份仍然未知。
最新一項(xiàng)研究中,研究人員采用小鼠模型,指出遺傳上剔除兩個(gè)新因子:TOX和TOX2,可以改善了CAR-T模型中針對(duì)黑色素瘤的根除。這項(xiàng)工作表明,針對(duì)患者的NR4A和TOX因子的干預(yù),可以將基于CAR-T的免疫療法的應(yīng)用范圍擴(kuò)展到實(shí)體瘤。
研究人員進(jìn)一步分析,表明TOX因子與NFAT和NR4A聯(lián)合起來能促進(jìn)PD-1抑制性受體的表達(dá),PD-1可以修復(fù)耗竭T細(xì)胞表面,發(fā)送免疫抑制信號(hào)。PD-1可以通過檢查點(diǎn)抑制劑這種單克隆抗體阻斷,這些抗體可抵抗免疫抑制,激活先天性抗癌免疫反應(yīng)。PD-1與TOX,NFAT和NR4A的合作令免疫抗癌更有意義,而且可以結(jié)合細(xì)胞免疫療法和抗體免疫療法。
如果通過用小分子治療CAR-T細(xì)胞來抑制TOX或NR4A,這種策略可能對(duì)黑色素瘤等實(shí)體癌癥有很強(qiáng)的治療作用。
Shoba Navai博士是貝勒醫(yī)學(xué)院,德克薩斯兒童醫(yī)院和休斯頓衛(wèi)理公會(huì)醫(yī)院的細(xì)胞和基因療法中心的兒科教授。她和她的同事使用靶向HER2的CAR-T細(xì)胞對(duì)10名復(fù)發(fā)/難治性HER+肉瘤患者進(jìn)行了治療。這些患者已經(jīng)接受過高達(dá)5次的補(bǔ)救性療法(salvage therapy)的治療,屬于非常難于治療的患者。
這項(xiàng)研究發(fā)現(xiàn),接受CAR-T療法的10名患者中有8名患者接受的CAR-T細(xì)胞在體內(nèi)增殖。其中一名患有橫紋肌肉瘤并且出現(xiàn)骨髓轉(zhuǎn)移瘤的兒科患者達(dá)到完全緩解(CR),緩解期持續(xù)了12個(gè)月后疾病復(fù)發(fā),再度接受CAR-T療法后她的CR已經(jīng)持續(xù)了17個(gè)月。另一名骨肉瘤兒科患者也達(dá)到完全緩解并且緩解期已經(jīng)達(dá)到32個(gè)月。

在紀(jì)念斯隆凱特琳癌癥中心的一項(xiàng)1期臨床研究中,研究人員使用名為lcasM28z的CAR-T細(xì)胞對(duì)惡性胸膜間皮瘤患者進(jìn)行治療。這種癌癥是一種侵襲性非常強(qiáng)的肺癌。LcasM28z是一種靶向間皮素(mesothelin)的CAR-T細(xì)胞療法,同時(shí)在細(xì)胞中加入了可以關(guān)閉CAR-T細(xì)胞功能的安全開關(guān)。
在這項(xiàng)試驗(yàn)中,21名患者接受了CAR-T療法的治療,在38周之后,其中13名患者的外周血中依然持續(xù)存在CAR-T細(xì)胞,而且這些患者體內(nèi)間皮素相關(guān)肽水平下降50%,并且成像研究顯示腫瘤出現(xiàn)縮小。

在癌癥疫苗領(lǐng)域,Imvax公司公布了該公司開發(fā)的創(chuàng)新自體腫瘤細(xì)胞疫苗IGV-001在1b期臨床試驗(yàn)中的積極結(jié)果。IGV-001是一款針對(duì)多形性膠質(zhì)母細(xì)胞瘤的腫瘤細(xì)胞疫苗。它將從患者大腦中切除的腫瘤組織與抑制腫瘤增生的反義分子混合,然后包裹在一個(gè)允許大分子滲出的滲透室(biodiffusion chamber)中植入患者的腹部。這會(huì)通過多種機(jī)制增強(qiáng)患者免疫系統(tǒng)對(duì)腫瘤抗原的反應(yīng)。在植入48小時(shí)之后,滲透室被取出,完成疫苗接種過程。這一創(chuàng)新疫苗已經(jīng)被美國(guó)FDA授予孤兒藥資格。
在這項(xiàng)試驗(yàn)中,患者接受不同劑量的疫苗接種,接種完成6-8周后,開始接受標(biāo)準(zhǔn)療法的治療。試驗(yàn)結(jié)果表明,接受最高劑量疫苗接種的患者,中位總生存期達(dá)到21.9個(gè)月,高于歷史上只接受標(biāo)準(zhǔn)療法患者的表現(xiàn)(14.6個(gè)月)。這些患者的PFS達(dá)到10.4個(gè)月,也高于只接受標(biāo)準(zhǔn)療法的患者(6.9個(gè)月)。

康奈爾醫(yī)學(xué)院的研究人員匯報(bào)了他們使用基于新抗原的癌癥疫苗治療林奇綜合癥(Lynch Syndrome)的臨床前結(jié)果。林奇綜合癥是一種遺傳性疾病,患者在一生中有70-80%的風(fēng)險(xiǎn)患上結(jié)直腸癌,同時(shí)患上其它類型癌癥的風(fēng)險(xiǎn)升高。林奇綜合征患者攜帶的基因突變阻礙DNA損傷修復(fù)的正常進(jìn)行,從而導(dǎo)致基因組中出現(xiàn)富集突變的編碼區(qū)微衛(wèi)星(coding microsatellite)。這些編碼區(qū)微衛(wèi)星能夠生成新抗原,它們可以被患者的免疫系統(tǒng)識(shí)別,但是通常不能激發(fā)足夠的免疫反應(yīng)來防止癌癥的發(fā)生。
研究人員對(duì)林奇綜合征患者的編碼區(qū)微衛(wèi)星進(jìn)行了篩選,并且找出能夠激發(fā)強(qiáng)力免疫反應(yīng)的新抗原作為腫瘤疫苗。在小鼠試驗(yàn)中,將這些腫瘤疫苗注射到模擬林奇綜合征的小鼠體內(nèi),能夠顯著降低小鼠腸道腫瘤負(fù)擔(dān),并且提高小鼠的生存期。未接受過疫苗接種的小鼠平均腸道腫瘤負(fù)擔(dān)為61 mg,總生存期為241天,而接受過疫苗接種的小鼠腸道腫瘤負(fù)擔(dān)為31 mg,總生存期為380天。
如何突破腫瘤微環(huán)境的障礙,讓CAR-T細(xì)胞療法發(fā)揮更廣泛的作用,很多科學(xué)家正在尋求不同的解決策略。
加州大學(xué)洛杉磯分校(UCLA)的顧臻教授和北卡大學(xué)教堂山分校Gianpietro Dotti教授帶領(lǐng)的研究團(tuán)隊(duì)想到了一種策略:通過給腫瘤定點(diǎn)“加熱”,以此加強(qiáng)CAR-T細(xì)胞的治療能力。將新興的光熱治療與CAR-T療法相結(jié)合,科學(xué)家們使黑色素瘤小鼠的腫瘤生長(zhǎng)在三周內(nèi)得到有效抑制,其中有1/3的小鼠在至少20天后體內(nèi)觀察不到腫瘤。這一最新成果本周在線發(fā)表于材料領(lǐng)域知名學(xué)術(shù)期刊《Advanced Materials》。
光熱治療和CAR-T療法相結(jié)合治療實(shí)體瘤
顧臻教授的研究團(tuán)隊(duì)致力于開發(fā)新型遞藥技術(shù)來助攻癌癥免疫治療,例如幾個(gè)月前,研究團(tuán)隊(duì)就開發(fā)出了噴涂在腫瘤部位的納米凝膠,用來抑制術(shù)后復(fù)發(fā)。

這一次,這支團(tuán)隊(duì)把光熱制劑包裹在可生物降解的高分子納米粒子內(nèi),局部注射到腫瘤部位。在使用近紅外激光照射后,光熱制劑可以把激光能量高效轉(zhuǎn)變?yōu)闊崮埽鼓[瘤部位得到局部加熱。
加熱的好處
一方面這種方法被證明可以部分破壞腫瘤細(xì)胞外的基質(zhì),擴(kuò)張血管促進(jìn)血流,直接促進(jìn)CAR-T在實(shí)體瘤內(nèi)的富集。另一方面,高溫對(duì)癌細(xì)胞的破壞會(huì)引起炎性反應(yīng),從而增強(qiáng)多種細(xì)胞因子的分泌,進(jìn)一步招募CAR-T并促進(jìn)CAR-T的激活。

研究人員在移植了人源黑色素瘤細(xì)胞的小鼠身上檢測(cè)了光熱治療與CAR-T療法相結(jié)合的效果。在將納米材料注入小鼠體內(nèi)的腫瘤后,通過調(diào)整激光照射時(shí)間和功率密度,同時(shí)輔以熱成像監(jiān)測(cè)來控制溫度,研究人員把腫瘤局部溫度升到40攝氏度。然后,再把具有特異性抗原的CAR-T細(xì)胞通過靜脈注入小鼠體內(nèi)。
對(duì)腫瘤的監(jiān)測(cè)結(jié)果顯示,結(jié)合光熱治療和CAR-T療法后,伴隨著CAR-T細(xì)胞在腫瘤部位的浸潤(rùn)和積累增加,小鼠體內(nèi)的腫瘤生長(zhǎng)在長(zhǎng)達(dá)20天的觀察期內(nèi)被顯著抑制。其中,有1/3接受結(jié)合治療的小鼠在20天結(jié)束實(shí)驗(yàn)時(shí)經(jīng)多種生化分析驗(yàn)證,體內(nèi)腫瘤已無法被檢測(cè)到。
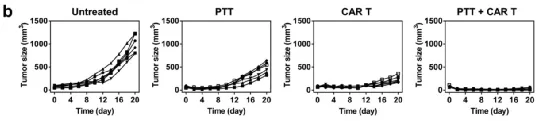
光熱療法和CAR-T細(xì)胞相結(jié)合,抑制了小鼠體內(nèi)的黑色素瘤生長(zhǎng)
方法:研究小組在注射了人類黑色素瘤腫瘤的老鼠身上測(cè)試了這項(xiàng)技術(shù)。他們將光熱劑注入腫瘤,然后用激光加熱。把激光的溫度提高到40℃有助于擴(kuò)張腫瘤賴以生長(zhǎng)的血管,從而增強(qiáng)T細(xì)胞進(jìn)入腫瘤的能力。最終再通過靜脈注射CAR-T細(xì)胞。
通過強(qiáng)化CAR-T細(xì)胞,該技術(shù)最終可改善難治性實(shí)體瘤患者的預(yù)后。接下來,研究人員將進(jìn)一步開展動(dòng)物實(shí)驗(yàn),以優(yōu)化加熱時(shí)間和溫度,再?zèng)Q定是否可以開展人體試驗(yàn)。
顧臻、Gianpietro Dotti教授團(tuán)隊(duì)帶來了這種解決CAR-T治療實(shí)體瘤的新思路,希望這種創(chuàng)新技術(shù)最終可以幫助更多癌癥患者改善預(yù)后。

西雅圖兒童醫(yī)院最近開展了一項(xiàng)名為STRIvE-01的嵌合抗原受體(CAR-T)細(xì)胞免疫治療試驗(yàn),該試驗(yàn)適用于伴有EGFR蛋白表達(dá)的實(shí)體瘤兒童和青少年患者。在第1階段試驗(yàn)中,雙靶標(biāo)的CAR-T細(xì)胞將更好地靶向兒童肉瘤、腎腫瘤和神經(jīng)母細(xì)胞瘤等實(shí)體腫瘤中的EGFR蛋白。
雖然在西雅圖兒童醫(yī)院的臨床試驗(yàn)中,CAR-T細(xì)胞在臨床試驗(yàn)中顯示出了治愈白血病兒童的希望,但在實(shí)體瘤上卻面臨更艱難的挑戰(zhàn)。實(shí)體腫瘤存在于特殊的微環(huán)境中,這些微環(huán)境有助于它們逃避免疫系統(tǒng),使得CAR-T細(xì)胞很難保持殺傷能力。
“為了使CAR-T療法能有效對(duì)抗實(shí)體腫瘤,我們不僅需要使CAR-T細(xì)胞進(jìn)入腫瘤微環(huán)境,還需要確保它們能夠存活并在那里茁壯成長(zhǎng)。”Albert博士說。
為了構(gòu)建STRIvE-01項(xiàng)目所需的CAR-T細(xì)胞,西雅圖兒童研究所Ben Towne兒童癌癥研究中心的Mike Jensen教授帶領(lǐng)研究團(tuán)隊(duì)將對(duì)患者的T細(xì)胞進(jìn)行重新編程,以靶向細(xì)胞表面表達(dá)異常的EGFR蛋白。在正常組織中,EGFR負(fù)責(zé)細(xì)胞生長(zhǎng)和發(fā)育。當(dāng)在惡性實(shí)體瘤中表達(dá)時(shí),EGFR則使腫瘤細(xì)胞更具侵襲性和侵入性。
通過使用名為EGFR806的抗體來武裝CAR-T細(xì)胞,研究人員希望選擇性地發(fā)現(xiàn)并破壞表達(dá)EGFR的實(shí)體瘤細(xì)胞,并限制其對(duì)正常組織的毒性。
“我們可能需要一系列治療策略來操縱免疫環(huán)境,才能治愈難以治療的實(shí)體瘤患者。”Albert博士說,“我很高興有機(jī)會(huì)將我們最先進(jìn)的免疫治療策略納入這次實(shí)體腫瘤治療計(jì)劃,我希望能為更多家庭提供最有效和最全面的CAR-T細(xì)胞治療方案,幫助治療孩子的癌癥。”
我國(guó)首個(gè)用于治療實(shí)體瘤的CAR-T細(xì)胞藥物獲批臨床試驗(yàn)
科濟(jì)生物首個(gè)CAR-T產(chǎn)品或臨床默示許可,靶向治療GPC3陽性實(shí)體腫瘤

2019年1月28日,科濟(jì)生物宣布,公司在研產(chǎn)品GPC3靶向的CAR-T細(xì)胞用于治療GPC3陽性實(shí)體腫瘤的臨床試驗(yàn)申請(qǐng)已通過了國(guó)家藥品監(jiān)督管理局藥品評(píng)審中心(CDE)的默示許可(受理號(hào)CXSL1700203),該許可也是我國(guó)首個(gè)用于治療實(shí)體瘤的CAR-T細(xì)胞藥物臨床試驗(yàn)許可。
公開資料顯示,2015年,上海交通大學(xué)醫(yī)學(xué)院附屬仁濟(jì)醫(yī)院發(fā)起了全球首個(gè)針對(duì)GPC3靶點(diǎn)治療晚期肝癌的探索性CAR-T臨床試驗(yàn),所用CAR-GPC3T細(xì)胞由科濟(jì)生物制備和提供。在2017年美國(guó)臨床腫瘤學(xué)會(huì)(ASCO)年會(huì)上,雙方公布了這一研究結(jié)果,首批參與研究的13名患者中,已經(jīng)有2名經(jīng)治療后3年所有腫瘤相關(guān)指標(biāo)完全正常。
另外,2018年9月8日,科濟(jì)生物在美國(guó)波士頓CAR-TCR峰會(huì)公布了CAR-T細(xì)胞治療胃癌/胰腺癌的臨床數(shù)據(jù):在接受治療的12名患者中,有8名患者出現(xiàn)不同程度腫瘤消退,特別是在一個(gè)經(jīng)過改良的治療亞組中,按照 RECIST 1.1標(biāo)準(zhǔn),6名患者有5名達(dá)到客觀緩解(其中1名待確認(rèn)客觀緩解),包括1名完全緩解。
自2018年3月,南京傳奇生物科技有限公司的CAR-T療法LCAR-B38M 成為我國(guó)首個(gè)獲批臨床試驗(yàn)的CAR-T細(xì)胞產(chǎn)品。值得一提的是,2018年,國(guó)內(nèi)已經(jīng)有7款CAR-T療法獲批臨床,進(jìn)入了臨床試驗(yàn)階段。而科濟(jì)生物在2018年有3款CAR-T產(chǎn)品的臨床申報(bào)獲得CDE受理。科濟(jì)生物的GPC3靶向的CAR-T細(xì)胞產(chǎn)品獲得臨床許可,是該公司首款獲得臨床默示許可的項(xiàng)目,也成為國(guó)內(nèi)第8個(gè)獲批臨床的CAR-T項(xiàng)目。
細(xì)胞治療領(lǐng)域的趨勢(shì)
最活躍細(xì)胞療法類型:CAR-T
文章顯示,共有1011個(gè)活躍的細(xì)胞療法,比一年前增加了258個(gè)。在不同的細(xì)胞療法類型中,CAR-T療法占據(jù)了半壁江山,達(dá)到568個(gè),比一年前顯著增加了164個(gè)。
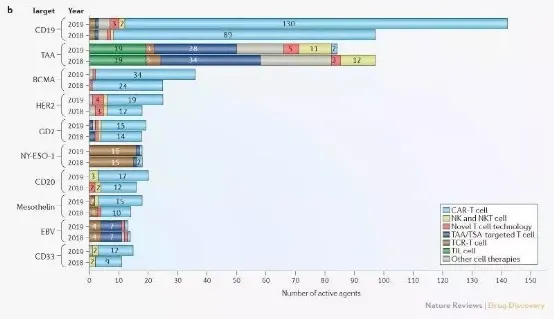
CD19是最熱門靶點(diǎn),其次是BCMA
142個(gè)細(xì)胞療法采用了CD19靶點(diǎn),其中包括130個(gè)CAR-T療法。B細(xì)胞成熟抗原(BCMA)是第二大最受歡迎的已定義靶點(diǎn),共36個(gè)在研療法,與去年相比增加了11個(gè),表明人們對(duì)BCMA越來越感興趣,這可能是由最近發(fā)布的多個(gè)有希望的臨床結(jié)果所推動(dòng)的。
美國(guó)和中國(guó)是主陣地
美國(guó)和中國(guó)在全球癌癥細(xì)胞治療領(lǐng)域處于領(lǐng)先地位,分別貢獻(xiàn)了439款和305款細(xì)胞療法,占全球的74%。
在研癌癥細(xì)胞療法地理分布:美國(guó)和中國(guó)領(lǐng)先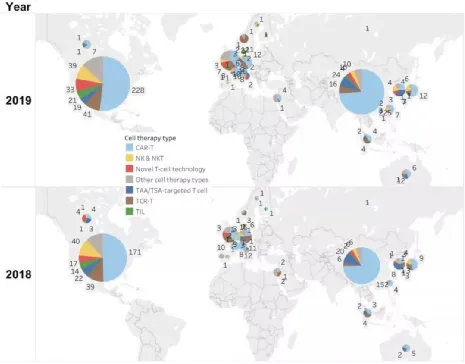
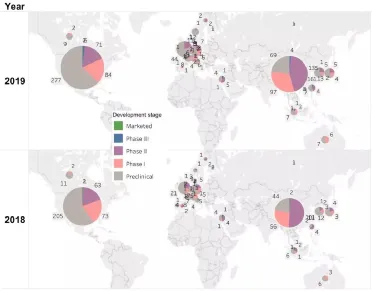
癌癥細(xì)胞療法在研階段比較
美國(guó)正在開發(fā)的大多數(shù)細(xì)胞療法都處于臨床前階段(63%; 277個(gè)),而中國(guó)目前正在開發(fā)的藥物大多處于臨床階段(77%; 236個(gè))。在過去一年中,全球范圍內(nèi)共增加26個(gè)新的臨床前細(xì)胞療法,有15個(gè)由美國(guó)開發(fā),而中國(guó)有3個(gè)。
?在研癌癥細(xì)胞療法臨床分期比較
臨床試驗(yàn)增長(zhǎng)迅速
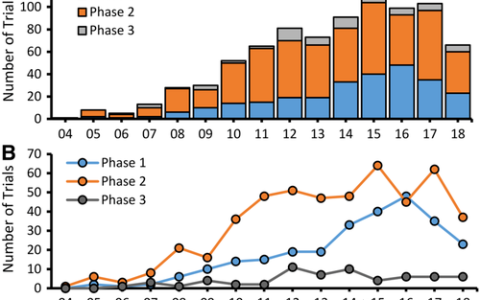
利用ClinicalTrials.gov數(shù)據(jù)庫,本文確定了自1993年至2019年3月,為測(cè)試癌癥細(xì)胞療法而開展的1216項(xiàng)臨床試驗(yàn)。這些數(shù)據(jù)表明,在過去的十年里,每年都有大量的新試驗(yàn)出現(xiàn),這主要是由于CAR-T療法的試驗(yàn)激增。
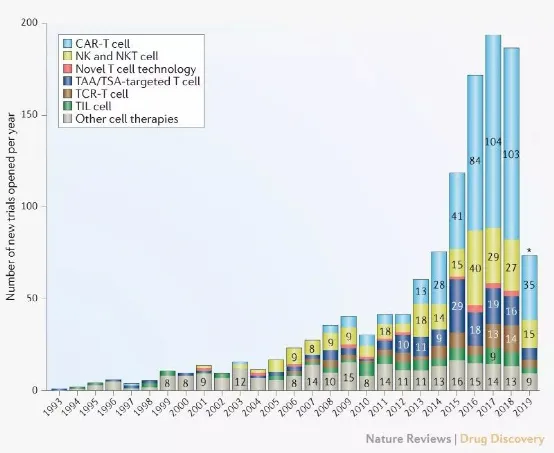
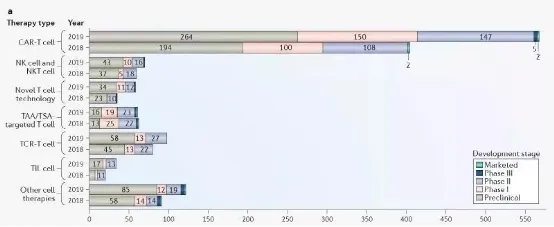
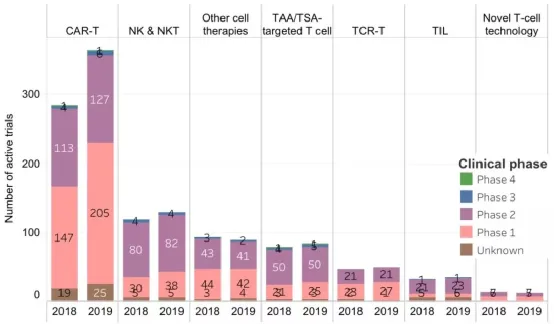
過去的一年(2018年3月至2019年3月)增加了96項(xiàng)活躍試驗(yàn),總計(jì)762項(xiàng),其中CAR-T療法的研究繼續(xù)占主導(dǎo)地位(在2019年3月正在進(jìn)行的有364項(xiàng))。數(shù)據(jù)還顯示,去年開展了188項(xiàng)新試驗(yàn),92項(xiàng)試驗(yàn)不活躍,表明這一領(lǐng)域的動(dòng)態(tài)性。
2018年至2019年間不同癌癥細(xì)胞療法類型的活躍試驗(yàn)
未來挑戰(zhàn):實(shí)體瘤細(xì)胞療法有待突破
雖然全球約90%的癌癥病例是實(shí)體腫瘤,但自1993年以來已開始的細(xì)胞治療試驗(yàn)中只有約一半(1,203項(xiàng)試驗(yàn)中的596項(xiàng))針對(duì)實(shí)體腫瘤,并且大多數(shù)針對(duì)實(shí)體瘤的細(xì)胞治療試驗(yàn)集中在少數(shù)腫瘤類型?– 如黑色素瘤(79項(xiàng)試驗(yàn))、大腦和中樞神經(jīng)系統(tǒng)癌癥(75項(xiàng)試驗(yàn))和肝癌(57項(xiàng)試驗(yàn)),許多實(shí)體瘤類型沒有進(jìn)行任何專門的細(xì)胞治療試驗(yàn)。
實(shí)體腫瘤和血液腫瘤細(xì)胞療法試驗(yàn)的比較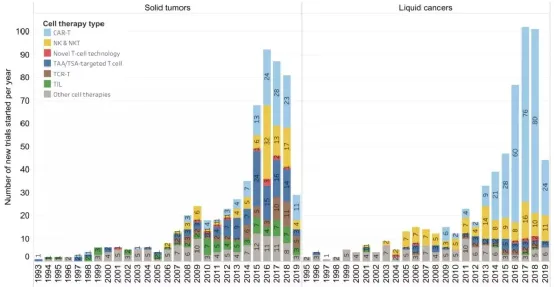
596個(gè)實(shí)體腫瘤試驗(yàn)的適應(yīng)癥總結(jié)
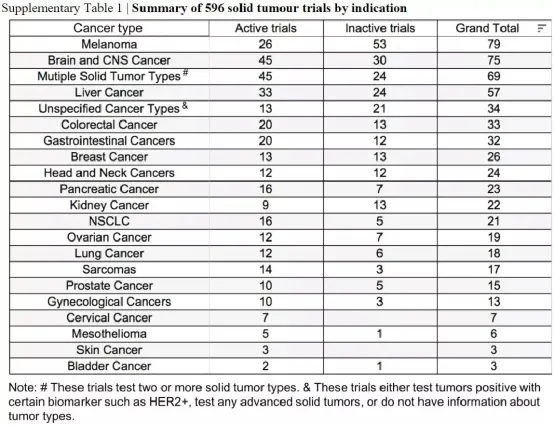
這些趨勢(shì)強(qiáng)調(diào)了細(xì)胞療法應(yīng)對(duì)實(shí)體瘤的更大挑戰(zhàn)。為了解決這些額外的困難,包括高抗原異質(zhì)性,強(qiáng)免疫抑制微環(huán)境和致密的細(xì)胞外基質(zhì),可能需要將細(xì)胞療法與其他免疫腫瘤藥物或癌癥藥物(如檢查點(diǎn)抑制劑)結(jié)合使用,為此正在進(jìn)行許多試驗(yàn)。
除CAR-T細(xì)胞之外的不同類型的細(xì)胞療法也可提供應(yīng)對(duì)某些挑戰(zhàn)的機(jī)會(huì)。實(shí)際上,雖然CAR-T療法的試驗(yàn)占所有血液惡性腫瘤試驗(yàn)的一半以上,但針對(duì)實(shí)體瘤的細(xì)胞療法試驗(yàn),在CAR-T和其他類型如NK細(xì)胞中的分布相當(dāng)均等。
最后,在活躍的臨床前細(xì)胞療法中,242個(gè)是專門針對(duì)實(shí)體腫瘤設(shè)計(jì)的,而172種是針對(duì)血液腫瘤設(shè)計(jì)的,這表明細(xì)胞治療領(lǐng)域?qū)?shí)體腫瘤的興趣日益濃厚。
展望
現(xiàn)在,細(xì)胞療法在免疫腫瘤學(xué)領(lǐng)域擁有最多的活躍在研候選產(chǎn)品、第二多的活躍試驗(yàn)(僅次于檢查點(diǎn)抑制劑)。過去一年的進(jìn)展表明,熱情仍在繼續(xù),例如更多的治療方案正在醞釀之中、更多的靶點(diǎn)正在探索之中、更多的試驗(yàn)開始了、更多的患者參與了試驗(yàn)。這些努力為臨床突破奠定了基礎(chǔ),使癌癥患者在不久的將來受益。
然而,重復(fù)現(xiàn)象一直在增加,例如CD19靶向CAR-T療法的增加以及測(cè)試某些可以說是多余療法的試驗(yàn)。因此,更多的努力需要探索CD19以外的靶點(diǎn),超越CAR-T療法的細(xì)胞療法,以及將CRISPR編輯的細(xì)胞療法和誘導(dǎo)多能干細(xì)胞等新技術(shù)整合到下一代細(xì)胞療法中,可能會(huì)帶來更大的進(jìn)展。此外,盡管實(shí)體瘤給癌癥患者帶來了巨大負(fù)擔(dān),但與相關(guān)臨床試驗(yàn)數(shù)量不匹配。通過使用創(chuàng)新的細(xì)胞療法和其他癌癥藥物如檢查點(diǎn)抑制劑的組合來治療實(shí)體腫瘤有望提供解決方案。
?
參考來源:
https://www.nature.com/articles/nrd.2018.167
https://www.nature.com/articles/d41573-019-00090-z
編輯:小果果,轉(zhuǎn)載請(qǐng)注明出處:http://www.448371.com/zixun/hybg/39293.html
免責(zé)聲明:本站所轉(zhuǎn)載文章來源于其他平臺(tái),主要目的在于分享行業(yè)相關(guān)知識(shí),傳遞當(dāng)前最新資訊。圖片、文章版權(quán)均屬于原作者所有,如有侵權(quán),請(qǐng)及時(shí)告知,我們會(huì)在24小時(shí)內(nèi)刪除相關(guān)信息。
說明:本站所發(fā)布的案例均摘錄于文獻(xiàn),僅用于科普干細(xì)胞與再生醫(yī)學(xué)相關(guān)知識(shí),不作為醫(yī)療建議。


 微信掃一掃
微信掃一掃  支付寶掃一掃
支付寶掃一掃