累趴的T細胞
每個人的身體內部都有一支隸屬于我們個人的專屬軍隊——免疫細胞,為保衛我們的健康沖鋒陷陣,萬死不辭。在眾多免疫細胞中,T細胞是不可或缺的一員大將。但T細胞也有累了的時候,我們如何理解“T細胞耗竭”?
我們通常所說的?T 細胞耗竭(T Cell Exhaustion)就是指,因長期慢性感染或癌癥,導致患者體內T細胞功能喪失的情況。由于長期暴露于持續性抗原或慢性炎癥,T細胞逐漸失去效應功能,記憶T細胞特征也開始缺失。T細胞耗竭是可以逆轉的,至少可以部分逆轉,主要是通過阻止PD-1之類的抑制性通路。

–01–

抗原的持續作用于T細胞耗竭
T細胞耗竭與抗原的持續驅動作用息息相關。感染后,初始T細胞經過抗原、共刺激和炎癥激活,以指數方式增殖形成效應T細胞亞群。
?
在急性感染或接種疫苗時,當炎癥消退或抗原清除后,某些效應T細胞會分化成功能性記憶T細胞,其可產生細胞因子(如IFN-γ、TNF和IL-2等),如同身經百戰的老兵,繼續巡邏在身體內。如果后續發生感染,很快產生強烈的免疫反應。
在慢性感染或癌癥期間,由于長期暴露于持續性抗原和炎癥,T細胞受到持續刺激,精疲力竭的效應T細胞逐漸失去效應功能,記憶T細胞特征也開始缺失,T細胞耗竭發生了。
?
耗竭T細胞(發生耗竭的T細胞)在功能上有別于效應T細胞和記憶T細胞,其特點是效應功能喪失,抑制性受體(IRS)表達增高且持續,表觀遺傳和轉錄譜改變,代謝方式改變。T細胞衰竭是癌癥病人免疫功能障礙主要因素之一。
T細胞是否會發生耗竭,主要受表達的抑制性受體(IRS)的水平和數量的影響,而免疫檢查點抑制劑可以部分逆轉T細胞耗竭狀態。此外,抗原刺激的強度和感染持續時間也是重要因素。
?
?
–02–
T細胞耗竭的機制概覽

(1)細胞間的信號(T細胞受體接合時間延長、共刺激和/或共抑制信號)
微環境影響可能包括組織分布和/或遷移模式改變,并導致感應氧張力的途徑(腫瘤抑制因子和/或缺氧誘導因子途徑)、pH和營養水平改變。組織破壞和淋巴組織改變可能起主要作用。
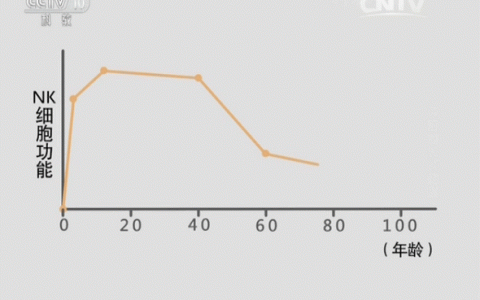
引起T細胞耗竭的原因可能是其他免疫細胞和基質細胞,除了CD8+T細胞耗竭參與已被證實,其他細胞包括:CD4+T細胞、NK細胞、抗原呈遞細胞(APC)、B細胞和調節細胞(例如骨髓來源的抑制細胞MDSC>和調節性T細胞Treg>)。
–03–
T細胞耗竭的調控因素
慢性感染或癌癥的一個關鍵特征:由于長期暴露于持續性抗原和炎癥,T細胞受到持續刺激。效應T細胞失去效應功能,記憶T細胞特征缺失。造成T細胞耗竭主要原因是:T細胞功能缺陷(免疫異型性受體表達增加,如PD-1、CTLA4、TIM-3),可溶性免疫抑制因子(如IL-10、IL-35增加),與其他免疫細胞的互動(如Treg細胞的抑制活性),共同造成了T細胞耗竭狀態。
新的證據也表明:耗竭T細胞表現出明顯的表觀遺傳特征,這可能導致對免疫治療的不良反應。抑制性受體表達增加是造成T細胞耗竭的主要原因,而免疫檢查點抑制劑可以部分逆轉T細胞耗竭狀態。
?
▉?PD-1/PD-LI

?
PD-1/PD-L1相互作用可誘導下游酪氨酸激酶(SYK)和磷酸酰基醇-3 激酶(PI3K)磷酸化,從而抑制下游信號傳導和T細胞的生物學功能,從而促進T細胞耗竭和凋亡;促進Treg細胞增殖和免疫抑制作用,抑制NK細胞和B細胞作用。
▉?PD-1/CTLA-4

?
CTLA-4激活磷脂酰肌醇激酶-3(PI3-K),造成T細胞功能喪失;CTLA-4結合TCR,導致條件性T細胞擴增,并將天然CD4+CD25+T細胞轉為Treg,從而抑制效應T細胞。

▉?IL-10
IL-10常與減弱T細胞活化有關,阻斷IL-10可預防和/或逆轉 T 細胞耗竭。DC細胞、B細胞、單核細胞、CD8+T細胞和非調節性CD4+T細胞都能產生IL-10。IL-10的作用可直接作用于T細胞,也可通過APC間接作用于T細胞,或兩者兼有。
–04–
如何遏制T細胞耗竭
▉?免疫檢查點抑制劑可逆轉T細胞耗竭狀態
耗竭T細胞表達免疫抑制性受體,免疫檢查點抑制劑可以阻斷這些信號,逆轉耗竭的T細胞,恢復腫瘤微環境腫瘤浸潤T細胞(TIL)功能。

T細胞耗竭的主要原因為免疫抑制性受體表達增加,如PD-1、CTLA-4、Tim-3等,聯合受體抑制劑治療可以增強免疫治療效果。
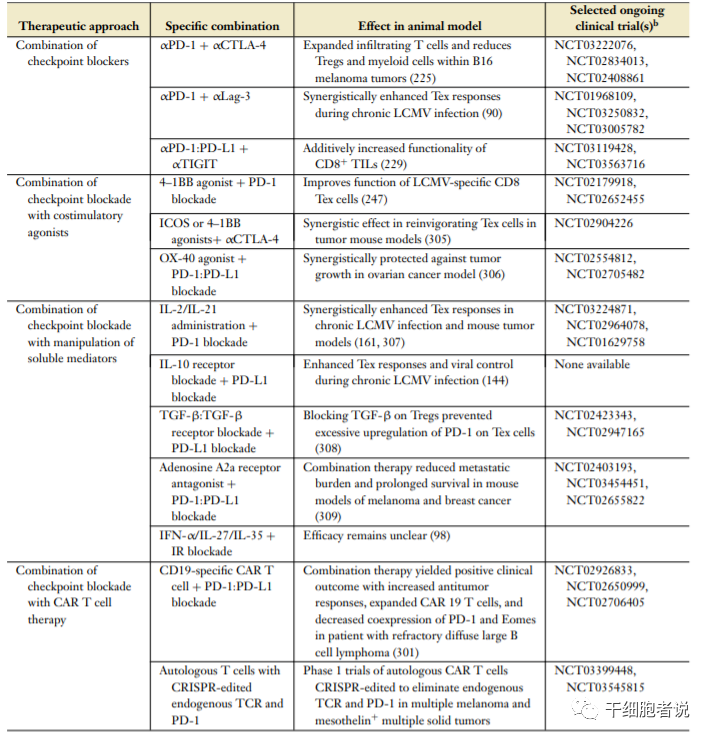 免疫聯合療法部分臨床試驗
免疫聯合療法部分臨床試驗–05–
文末的話
T細胞衰竭機制復雜,因素眾多。根本原因還是抗原和炎癥長期刺激 T 細胞,T細胞厭倦了這樣的生活,開始躺平,不愿意搭理這些抗原或炎癥,效應T細胞不再效應,記憶T細胞也不再記憶。
?
其實,人何嘗不是如此。當你長期處于焦慮狀態,體內源源不斷給你提供免疫抑制劑和神經抑制劑,你的免疫系統和神經系統將持續低下。雖然我無法證實這件事,但人還是要開心一點,遠離焦慮!耗竭的T細胞就是榜樣。
參考文獻:
-
http://www.bloodjournal.org/Thorsten?Zenz -
Annu. Rev. Immunol. 2019. 37:457–95 -
Nature Reviews Clinical Oncology, 2016, 13(4):202-203. -
Nat Immunol.?2013 Dec;14(12):1212-8. -
Nat Metab?2,?1001–1012(2020).? -
Annu Rev Immunol.?2019 Apr 26;37:457-495.
編輯:小果果,轉載請注明出處:http://www.448371.com/cells/myxb/13103.html
免責聲明:本站所轉載文章來源于其他平臺,主要目的在于分享行業相關知識,傳遞當前最新資訊。圖片、文章版權均屬于原作者所有,如有侵權,請及時告知,我們會在24小時內刪除相關信息。
說明:本站所發布的案例均摘錄于文獻,僅用于科普干細胞與再生醫學相關知識,不作為醫療建議。


 微信掃一掃
微信掃一掃  支付寶掃一掃
支付寶掃一掃